
| A、向AlCl3中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| B、硫酸氢钠溶液中加入足量的烧碱溶液:H++OH-=H2O |
| C、过氧化钠加入水:2Na2O2+2H2O=4OH-+O2↑+4Na+ |
| D、金属铝溶于氢氧化钠溶液:2Al+2OH-=2AlO2-+H2↑ |


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
| A、n(Fe)<n(S),总质量等于44g |
| B、n(Fe)>n(S),总质量等于44g |
| C、n(Fe)=n(S),总质量大于44g |
| D、n(Fe)<n(S),总质量大于44g |
查看答案和解析>>
科目:高中化学 来源: 题型:
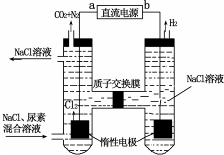
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SnCl4、Fe2(SO4)3 |
| B、Fe2(SO4)3、SnCl4 |
| C、SnCl2、FeSO4、 |
| D、HCl、H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能说明非金属性Cl>C:2HCl+CaCO3═CaCl2+CO2↑+H2O |
| B、能说明氧化性H2O2>Fe3+:2Fe2++H2O2+2H+═2Fe3++2H2O |
| C、已知:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1(稀溶液),能说明稀硫酸与NaOH稀溶液反应生成1mol水,放出的热量为57.3 kJ |
| D、能说明CH3COOH是弱电解质:CH3COO-+H2O?CH3COOH+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 叙述 | 推论 | |
| A | 酸性:HCl>H2CO3>H2SiO3 | 非金属性:Cl>C>Si |
| B | 组成原电池时,通常是还原性较强的物质做负极 | 镁和铝在氢氧化钠溶液中组成原电池时,镁做负极 |
| C | -OH是亲水基,含有-OH的有机物都易溶于水 | 常温时,C2H5OH和 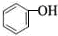 都易溶于水 都易溶于水 |
| D | 溶解度小的沉淀可转化成溶解 度更小的沉淀 | 向AgCl悬浊液中滴加KI溶液可以得到AgI沉淀 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、漂白粉长期暴露在空气中会变质失效 |
| B、雾霾天车灯照射的光亮通路属于丁达尔现象 |
| C、硬铝属于合金材料,瓷器属于硅酸盐制品 |
| D、不锈钢具有较强的抗腐蚀性,是因为在钢铁表面镀上了金属铬 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、卤化氢中,以HF沸点最高,是由于HF分子间存在氢键 |
| B、H2O的沸点比HF的高,是由于水中形成的氢键多 |
| C、氨水中有分子间氢键 |
| D、氢键X-H…Y的三个原子总在一条直线上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com