
 常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LNaOH溶液.整个实验过程中溶液的pH变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LNaOH溶液.整个实验过程中溶液的pH变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是( )| A. | 实验过程中用pH试纸测定溶液的pH | |
| B. | a~b段,溶液中 $\frac{c({H}^{+})}{c(O{H}^{-})}$ 减小 | |
| C. | b点对应溶液中:c(Cl-)>c(H+)>c(HClO)>c(ClO-)>c(OH-) | |
| D. | c点对应溶液中:c(Na+)=c(Cl-)+c(ClO-) |
分析 A.氯气与水反应生成次氯酸,次氯酸具有漂白性;
B.氯气与水反应生成氯化氢和次氯酸,氯化氢完全电离生成氢离子,溶液酸性增强;
C.氯气与水反应生成等物质的量的氯化氢和次氯酸,氯化氢为强电解质,次氯酸为弱电解质;
D.依据溶液中电荷守恒解答;
解答 解:A、氯气和氢氧化钠反应生成氯化钠和次氯酸钠,次氯酸钠有强氧化性,能漂白,所以不能测其pH值,故A错误;
B、氯气与水反应生成氯化氢和次氯酸,氯化氢完全电离生成氢离子,所以从a到b溶液酸性增强,溶液的pH逐渐变小,说明氢离子和氢氧根离子浓度比值变小,故B错误;
C、b点是氯水的饱和溶液,由于氯化氢和次氯酸都电离产生氢离子,所有氢离子浓度比氯离子浓度大,故C错误;
D、根据电荷守恒,在c点溶液为中性,氢离子浓度等于氢氧根离子浓度,则c(Na+)=c(Cl-)+c(ClO-),故D正确;
故选:D.
点评 本题考查了氯水性质,熟悉氯水成分,明确微粒具有性质是解题关键,注意电荷守恒在判断离子浓度大小的应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了保持腊肉肉质鲜美,添加过量的亚硝酸钠 | |
| B. | 为了防止食用鱿鱼变质,用甲醛水溶液浸泡存放 | |
| C. | 为了防止黄曲霉素对人体的危害,绝对不能食用霉变食物 | |
| D. | 为了防止摄入锌不足引起疾病,过量服用补锌药剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(h) 物质的量/(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
查看答案和解析>>
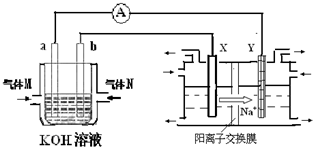
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
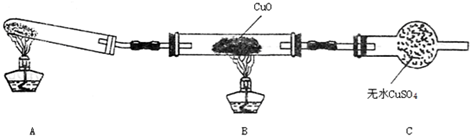
科目:高中化学 来源: 题型:解答题
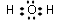 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
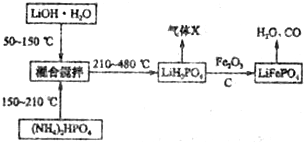
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com