
将纯水加热至较高温度,下列叙述正确的是
| A.水的离子积变大、pH变小、呈酸性 | B.水的离子积不变、pH不变、呈中性 |
| C.水的离子积变小、pH变大、呈碱性 | D.水的离子积变大、pH变小、呈中性 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
化学与生活、社会密切相关,下列说法正确的是 ( )
| A.合金的许多性能优于其组成成分,如硬度都会增大,熔点都会升高 |
| B.要除去衣服上的顽固污渍,可将衣服泡在漂白液中 |
| C.硅是地壳中含量位居第二的元素,其中玛瑙、光导纤维的主要成分为SiO2 |
| D.工业上获得大量的乙烯、丙烯、丁二烯的方法是石油裂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L H2SO4溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
若实验中大约要使用245 mL NaOH溶液,则至少需要称量NaOH固体________g。
Ⅱ.测定中和热的实验装置如图所示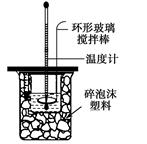
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值57.3 kJ/mol):________ 。
(2)取50 mL NaOH溶液和30 mL硫酸进行实验,实验数据如下表。
①请填写下表中的空白: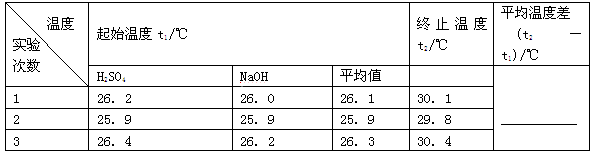
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L H2SO4溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH=________(取小数点后一位)。
③上述实验结果的数值与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)________。
a.实验装置保温、隔热效果差
b.在量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
当氢氧化镁固体在水中达到溶解平衡Mg(OH)2(s)  Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,须加入少量的
Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,须加入少量的
| A.MgCl2 | B.NaOH | C.MgSO4 | D.NaHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙(其pH变色范围为3.1~4.4)作指示剂,下列操作中可能使测定结果偏低的是
| A.酸式滴定管在装酸液前未用标准盐酸润洗2~3次 |
| B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 |
| C.锥形瓶溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度 |
| D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列电离方程式错误的是
| A.(NH4)2SO4溶于水:(NH4)2SO4===2NH4++SO42- |
| B.H3PO4溶于水:H3PO4===3H++PO43- |
C.HF溶于水:HF H++F H++F |
D.NaHS溶于水:NaHS===Na++HS-,HS- H++S2- H++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(4分)在25℃时,有pH为a的HCl溶液和pH为b的NaOH溶液,取VaL该盐酸溶液用该NaOH溶液中和,需VbL NaOH溶液,(题中a≤b,b≥8)。问:
(1)若a+b=14,则Va/Vb= .
(2)若a+b=13,则Va/Vb=
(3)若a+b>14,则Va/Vb= ,且Va Vb(填“>”“<”“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com