
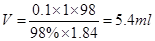 。
。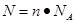 、n=m/M、
、n=m/M、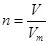 、
、 ,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。例外还需要注意分子的个数和原子的个数是不同的,计算时需要分清楚。
,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。例外还需要注意分子的个数和原子的个数是不同的,计算时需要分清楚。

科目:高中化学 来源:不详 题型:计算题
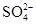 的物质的量浓度是 。
的物质的量浓度是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶 |
| B.用托盘天平准确称取所需的Na2CO3?10H2O晶体的质量,放入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解 |
| C.将已冷却的溶液沿玻璃棒注入250mL的容量瓶中 |
| D.将容量瓶盖紧,振荡,摇匀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③④ | B.②③⑥⑦ | C.①②④⑤ | D.②③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.012 kg 12C含有的碳原子数就是阿伏加德罗常数 |
| B.6.02×1023就是阿伏加德罗常数 |
| C.含有阿伏加德罗常数个粒子的物质的量是1 mol |
| D.1 mol NH3所含原子数约是2.408×1024 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com