
����Ŀ��������A���緢������ţ���У������������Ǵ�л���м��壬�����������������۵ȷ����Ƶá�A�ĸ���������ϲ���IJ��Ƽ�֮һ��A��ij�ִ��������½�������������ﲻ�ܷ���������Ӧ����Ũ��������£�A�ɷ�������ͼ��ʾ�ķ�Ӧ��

��1����д��������Ľṹ��ʽ��A_____________��E_____________��F_____________��
��2����ѧ����ʽ��A��B:______________________________________��
��3���ĸ���Ӧ�У�������������Ӧ���ǣ�A��_________(������Ӧ����ĸ)
���𰸡�
��1��CH3CH(OH)COOH��CH2=CHCOOH�� ��
��
��2��CH3CH(OH)COOH+CH3CH2OH![]() CH3CH(OH)COOCH2CH3+H2O��
CH3CH(OH)COOCH2CH3+H2O��
��3��E��
��������
���������A��Ũ��������¼��ܺ��Ҵ���Ӧ�����ܺ����ᷴӦ��˵��A�м����Ȼ������ǻ���A�������IJ��ﲻ�ܷ���������Ӧ��˵���ǻ�����̼���Ķ˵��ϣ����ж�AΪCH3CH(OH)COOH����A�������ɵ�CH3COCHO�����ܷ���������Ӧ��A���Ҵ�����������Ӧ����BΪCH3CH(OH)COOCH2CH3��A�����ᷢ��������Ӧ����DΪCH3COOCH(CH3)COOH��A��Ũ���ᡢ��������������E��E������ˮ��ɫ��Ӧ������ȥ��Ӧ����EΪCH2=CHCOOH��A��Ũ���ᡢ����������������ԭ�ӻ�״������F�����F�ķ���ʽ��֪��Ϊ2����A����������Ӧ���ɻ�״�������FΪ ��
��
��1����������������AΪCH3CH(OH)COOH��EΪCH2=CHCOOH��FΪ ���ʴ�Ϊ��CH3CH(OH)COOH��CH2=CHCOOH��
���ʴ�Ϊ��CH3CH(OH)COOH��CH2=CHCOOH�� ��
��
��2��A��B����ѧ����ʽΪCH3CH(OH)COOH+CH3CH2OH![]() CH3CH(OH)COOCH2CH3+H2O���ʴ�Ϊ��CH3CH(OH)COOH+CH3CH2OH
CH3CH(OH)COOCH2CH3+H2O���ʴ�Ϊ��CH3CH(OH)COOH+CH3CH2OH![]() CH3CH(OH)COOCH2CH3+H2O��
CH3CH(OH)COOCH2CH3+H2O��
��3���ĸ���Ӧ�У�������������Ӧ���ǣ�A��E��������ȥ��Ӧ���ʴ�Ϊ��E��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25�� Ksp��Ag2S��=6.3��10��50��Ksp��AgCl��=1.5��10��16��ɳ����ѧij�о���ѧϰС��̽��
AgCl��Ag2S����ת����ԭ��
�� �� | �� �� |
��NaCl��AgNO3��Һ��� | ������ɫ���� |
�������ù�Һ������м�Na2S��Һ | ������Ϊ��ɫ |
���˳���ɫ����������NaCl��Һ | �ϳ�ʱ�������Ϊ���ɫ |
��1�����еİ�ɫ������ ��
��2��������˵��������ڵĵ����ӷ���ʽ�� ������ת������Ҫԭ���� ��
��3���˳�����������ɫ�������Ʋ⺬��AgCl����ŨHNO3�ܽ⣬��������ɫ���壬���ֳ���δ��
�⣬���˵õ���ҺX�Ͱ�ɫ����Y��
������X�еμ�Ba��NO3��2��Һ��������ɫ����
������Y�еμ�KI��Һ��������ɫ����
���ɢ��жϣ���ҺX�б������������ ��
���ɢ�������ȷ�ϲ���������ɫ��������AgCl����һ�ֳ���_____ _��
��4����ѧ��ͨ�����¶���ʵ��ȷ���˲������ ���ɫ����������ԭ����NaCl�����£����������к�ɫ����������

�� �� | B��һ��ʱ��������ɫ���� |
C��һ��ʱ��������Ա仯 |
��A�����������_________��
��C��ʢ�ŵ�����W��_________��
�۸�ͬѧ��ΪB�в��������ķ�Ӧ���£��벹����������
2Ag2S + ![]() +
+ ![]() + 2H2O
+ 2H2O ![]() 4AgCl +
4AgCl + ![]() + 4NaOH
+ 4NaOH
�ܴ�ƽ���ƶ��ĽǶȣ�����B��NaCl�����ã� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��M��NΪ�����ڵĵ���������Ԫ�ء�����X��Zͬ���壬Y��Zͬ���ڣ�M��X��Y�Ȳ�ͬ���壬Ҳ��ͬ���ڡ�Xԭ�������������Ǻ�����Ӳ�����������Y������ϼ�������ͻ��ϼ۵Ĵ����͵���6��N�Ƕ���������Ԫ����ԭ�Ӱ뾶���ķǽ���Ԫ�ء�
��1��XԪ��λ��Ԫ�����ڱ���λ���ǵ� ���ڣ��� ��
��2����д�����з�Ӧ�����ӷ���ʽ��N����������������Һ��Ӧ��
��3��Y��Z��ȣ��ǽ����Խ�ǿ��Ԫ�ص�ԭ�ӽṹʾ��ͼΪ ������֤���ý��۵�ʵ���ǣ������ӷ���ʽ��ʾ�� ��
��4���뽫X��Z��M��NԪ��ԭ�Ӱ뾶�Ӵ�С���� ����Ԫ�ط��ű�ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���������е�����Ϊ42��
��1���������ķ���ʽΪ________________________��
��2��д�����������ӵ�����ͬ���칹��Ľṹ��ʽ��_________________________��
��3������ͬ���칹���У�����ͬ�����·е���͵���____________(д�ṹ��ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���мס�����λͬѧ��������ԭ��ط�Ӧ�������Ļ��˳�����˾���þƬ����Ƭ���缫������ͬѧ���缫����6 mol��L��1��H2SO4��Һ�У���ͬѧ���缫����6 mol��L��1��NaOH��Һ�У���ͼ��ʾ��
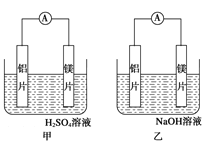
��1��д�����������ĵ缫��Ӧʽ_____________________________��
��2��д����������ܷ�Ӧ�����ӷ���ʽ�� ___________________��
��3�����������ͬѧ����Ϊ������ԭ��صĵ缫����������ǽ������ɸ������ϵĽ���Ӧ�ȹ����������ϵĽ������á�������жϳ�________����дԪ�ط��ţ���ͬ���Ľ��������ǿ�����һ��жϳ�________�Ľ�����Ը�ǿ��
��4���ɴ�ʵ����������������Щ��ȷ����
A������ԭ��ط�Ӧ�жϽ������˳��ʱӦע��ѡ����ʵĽ���
B��þ�Ľ�����Բ�һ�������Ľ������ǿ
C����ʵ��˵���������˳����ѹ�ʱ����û��ʹ�ü�ֵ
D����ʵ��˵����ѧ�о������ӡ���Ӧ������Ӱ��ϴ����Ӧ��������������
��5������ʵ��Ҳ������֤���ˡ�ֱ�����ý������˳���ж�ԭ����е�������������������_________(��ɿ������ɿ���)���粻�ɿ������������һ���ж�ԭ������������Ŀ���ʵ��___________ (��ɿ����ɲ���д)��
��6����5.1gþ���Ͻ�����60mL 5.0 mol��L��1H2SO4��Һ�У���ȫ�ܽ���ټ���65mL 10.0mol��L��1��NaOH��Һ���õ�����������Ϊ9.7g�������μ�NaOH��Һʱ��������١�
�������� mL NaOH��Һʱ����ʹ�ܽ��������Mg2+��Al3+ǡ����ȫ������
���Ͻ���������ʱ�������������ڱ�״���µ����Ϊ L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڳ����£������й���Һ����Ũ�ȹ�ϵ��������ȷ����
A����0.1mol/LNH4Cl��Һ��ͨ��һ����������c(Cl-)��c(NH4+)��c(OH-)��c(H+)
B�����е����ʵ�����NaClO��NaHCO5����Һ�У�c(HClO)+c(ClO-)�Tc(HCO3-)+c(H2CO3)+2c(CO32-)
C����CH3COONa��Һ�еμ�ϡHCl��pH=7��c(Na+)��c(Cl-)=c(CH3COOH)
D������������ʵ���Ũ��CH3COOH��Һ��CH3COONa��Һ��ϣ�
2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪700��ʱ��H2(g)+CO2(g)![]() H2O(g)+CO(g)�����¶��£��ڼס��ҡ������������ܱ������У�Ͷ��H2��CO2����ʼŨ�����±���ʾ�����м�2min��ƽ��ʱ��v(H2O)Ϊ0.025mol/(Lmin)�������жϲ���ȷ����( )
H2O(g)+CO(g)�����¶��£��ڼס��ҡ������������ܱ������У�Ͷ��H2��CO2����ʼŨ�����±���ʾ�����м�2min��ƽ��ʱ��v(H2O)Ϊ0.025mol/(Lmin)�������жϲ���ȷ����( )
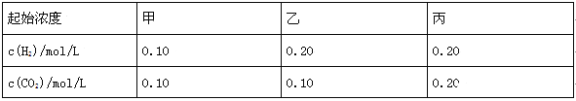
A��ƽ��ʱ������CO2��ת���ʴ���50%
B������Ӧƽ��ʱ������c(CO2)�Ǽ��е�2��
C���¶�����800����������Ӧƽ�ⳣ��Ϊ![]() ��������ӦΪ���ȷ�Ӧ
��������ӦΪ���ȷ�Ӧ
D�������������䣬����ʼʱ���������г���0.10mol/L H2��0.20 mol/L CO2������ƽ��ʱc (CO)��ԭ��������ƽ��ʱc (CO)��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2015��8��12�գ�������������ը�¹�ȷ�����軯��(NaCN)���������Ƶ����軯�����Ժ�ǿ����ˮ���������ж���ȼ�軯�����塣�軯��ķе�ֻ��26���϶ȣ�����൱���ӷ������������ʹ���������ж��ķ��ա�ͬʱ�軯�������������ƻᷢ����ը���ش���������
��1��д���軯����ˮ�����軯������ӷ���ʽ
��2����ը�ֳ�Լ700�ֵ��軯�ƴ�Լ��Ҫ900�ֵ�˫��ˮ���������軯����˫��ˮ�������ͷų�����ͬʱ������ɫ����̼�����ƣ�ʹ���軯�ƵĶ��Դ�ͣ�д���軯����˫��ˮ��Ӧ�Ļ�ѧ����ʽ ��
��3���軯�������������������������ƺ���������Ⱦ�����巢����ը��д����ѧ��Ӧ����ʽ ��
��4����ը�����ڷ�ˮ�е�CN- ������Cr2O72-�������ⶨ�������̽��з�ˮ����,
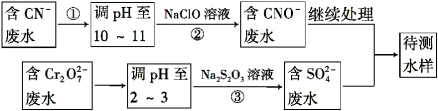
�� ����������ˮ��������Ҫʹ�õķ����� ��
A�������� B���кͷ� C�������� D��������ԭ��
�� ����ڷ�Ӧ������ų�,�÷�Ӧ�����ӷ���ʽΪ_______________________��
�� �������,ÿ����0.4 mol Cr2O72 - ʱת�Ƶ���2.4 mol,�÷�Ӧ�����ӷ���ʽΪ ___________��
�ܴ�������Cr2O72-��ˮ������������巨���÷������ˮ�м���FeSO4��7H2O��Cr2O72-��ԭ��Cr3+,����pH,Fe��Crת�����൱��Fe��[Fex��Cr(2-x)��]O4(��������,�������ֱ�ʾԪ�ؼ�̬)�ij���������1 mol Cr2O72-,�����amol FeSO4��7H2O,���н�����ȷ���� ��
A��x=0.5,a=6 B��x=0.5,a=10 C��x=1.5,a=6 D��x=1.5,a=10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ������װ���Ʊ�������Cl2�����ʡ�
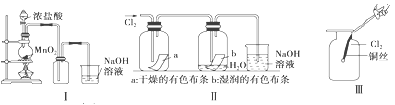
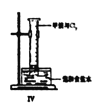
��1����ͼԲ����ƿ�з�Ӧ�Ļ�ѧ����ʽ��
��2����ͼ����ɫ���� ����a��b�����ձ��з�Ӧ�����ӷ���ʽ��
��3����Cu˿����Fe˿������ʵ�飬���Ҳ�ܵ�ȼ������ΪFe˿Ҳ�ɵ�ȼ����ȷ�е������� ��
A��Fe��Cu���ǽ���Ԫ�� B��Fe���۵��Cu��
C��Fe���ܶȱ�CuС D��Fe�Ľ����Ա�Cuǿ
��4������װ�÷����ڹ����ĵط����չ�û��ֱ����������һ����۲쵽��Ͳ��������״Һ�����ɣ���Ͳ��Һ����������״Һ�εijɷֿ����ǣ�д����ʽ�� ����Ͳ��Һ����������Ҫԭ����_________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com