
下列离子方程式正确的是
A.将过量NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++HCO3-+OH—==CaCO3↓+H2O
B.Fe(OH)3溶于氢碘酸: Fe(OH)3 + 3H+ ==Fe3+ + 3H2O
C.向硫酸铝铵[NH4Al(SO4)2]溶液中加入氢氧化钡溶液至SO42ˉ离子沉淀完全Al3+ + 2SO42ˉ + 2Ba2+ + 4OHˉ ==Al(OH)4ˉ + 2BaSO4↓
D.向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热:Ba2++ 2OH-+NH4++ HCO3- NH3↑+2H2O+BaCO3↓
NH3↑+2H2O+BaCO3↓
科目:高中化学 来源:2015-2016学年江苏省泰州市姜堰区高二上学期期中选修化学试卷(解析版) 题型:填空题
用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl(g)+O2(g)  2Cl2(g)+2H2O(g)。
2Cl2(g)+2H2O(g)。
(1)研究表明反应A通过如下图所示的催化剂循环实现。
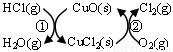
反应①为:2HCl(g)+CuO(s) H2O(g)+CuCl2(g) ΔH1
H2O(g)+CuCl2(g) ΔH1
反应②生成1 mol Cl2(g)的反应热为ΔH2,则A反应的反应热表示为 。(用ΔH1和ΔH2表示)。
(2)反应A中,4mol HCl被氧化,放出115.6kJ的热量,且部分化学键断裂示意图如下:

①H2O的电子式是 ,反应A的热化学方程式是 。
②断开1 mol H—O键与断开 1 mol H—Cl 键所需能量相差约为 kJ,H2O中H—O 键比HCl中H—Cl键 (填“强”或“弱”)。
(3)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性。
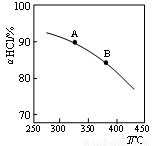
实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的ɑHCl—T曲线如上图所示,若压缩体积使压强增大,画出相应ɑHCl—T曲线的示意图,并简要说明理由 。
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰市宁城县高三上学期第一次统考化学试卷(解析版) 题型:填空题
煤是一种重要的化工原料,人们将利用煤制取的水煤气、焦炭、甲醚等广泛用于工农业生产中。
(1)已知:
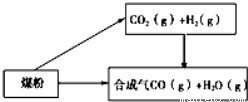
①C(s)+H2O(g)═CO(g)+H2(g) △H=+131.3kJ·mol﹣1
②CO2(g)+H2(g)═CO(g)+H2O(g) △H=+41.3kJ·mol﹣1
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为 。
该反应在 (填“高温”、“低温”或“任何温度”)下有利于正向自发进行.
(2)有人利用炭还原法处理氮氧化物,发生反应C(s)+2NO(g) N2(g)+CO2(g).向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
N2(g)+CO2(g).向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
| 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①10~20min内,N2的平均反应速率v(N2)= .
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是__________(填字母序号).
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明:反应CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020mol·L﹣1,在该条件下达到平衡时,CO的转化率为 .
(4)用CO做燃料电池电解CuSO4溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
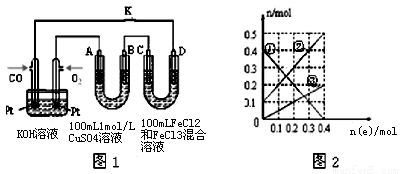
①乙中A极产生的气体在标准状况下的体积为 .
②丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,则图中③线表示的是 (填离子符号)的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要 mL 5.0mol·L﹣1 NaOH溶液.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列各组离子在满足指定条件下,能大量共存的是
A.无色溶液:Cu2+、K+、Cl-、CO32-
B.使酚酞显红色的溶液:Mg2+、Fe2+、Cl-、SO42-
C.加Fe粉能产生H2的溶液:Ba2+、Na+、Cl-、SO42-
D.加盐酸能产生气体的溶液:Na+、K+、NO3-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期半期考试化学试卷(解析版) 题型:选择题
由1-丙醇制取 ,最简便的流程需要下列反应的顺序应是
,最简便的流程需要下列反应的顺序应是
a.氧化 b.还原 c.取代 d.加成 e.消去 f.中和 g.缩聚 h.酯化
A.b、d、f、g、h B.e、d、c、a、h
C.a、e、d、c、h D.b、a、e、c、f
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列各项中,理由、结论及因果关系均正确的是
选项 | 理由 | 结论 |
A | 键能:N≡N>Cl-Cl | 单质沸点:N2>Cl2 |
B | 分子中可电离的H+个数:H2SO4>CH3COOH | 酸性:H2SO4>CH3COOH |
C | 元素的金属性:K>Na | 碱性:KOH>NaOH |
D | 氧化性:Fe3+>Cu2+ | 还原性:Fe2+>Cu |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省扶余市高一上学期期中测试化学试卷(解析版) 题型:填空题
若在相同温度压强下,对于氨气(NH3)和硫化氢(H2S)气体:
(1)等质量的氨和硫化氢气体的体积比为 ;
(2)等体积的氨气和硫化氢气体的质量比为 ;
(3)若二者氢原子数相等,则它们的体积比为 ;
(4)硫化氢的密度是氨气的 倍。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省三门峡市高二上学期期中测试化学试卷(解析版) 题型:填空题
在氢氟酸溶液中,存在如下电离平衡:HF H++F﹣
H++F﹣
(1)加入固体NaOH,电离平衡向 反应方向移动,c(H+) .
(2)加入固体NaF,电离平衡向 反应方向移动,c(H+) .
(3)升高温度,电离平衡向 反应方向移动,c(H+) .
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期期中测试理综化学试卷(解析版) 题型:填空题
有X、Y、Z、R四种短周期主族元素,Y、Z、R同周期。相关信息如下:
相关信息 | |
X | 单质为双原子分子。若低温蒸发液态空气,因其沸点较低可先获得X的单质 |
Y | 含Y元素的物质焰色反应为黄色 |
Z | 同周期元素中原子半径最小 |
R | R元素原子的最外层电子数是K层电子数的3倍 |
I.(1)Z元素在周期表的位置是 ,Y、Z、R简单离子的半径从大到小的顺序是 (用离子符号表示);
(2)由X、Z两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里X、Z两种原子最外层均达到8个电子的稳定结构。甲遇水可形成一种常见的漂白性物质。则甲的结构式为 ;
(3)化合物乙(Y2R)溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Y2R2,其溶液显黄色。则Y2R2的电子式为 ,写出乙溶液在空气中变质生成Y2R2的化学方程式 。
II.元素X与氢可形成多种化合物,如丙、丁、戊。
(4)丙为一元弱酸,酸性与醋酸类似,对热十分稳定但受撞击就爆炸。8.6 g丙爆炸分解生成H2和6.72 L(标况下)X2。写出其爆炸的化学方程式 ;
(5)丁为离子化合物,遇水反应生成H2和气体戊,标况下戊的密度为0.76 g·L-1,则物质丁的化学式为 ;
(6)戊在高温条件下能还原Fe2O3,生成两种单质,写出该反应的化学方程式 ,有人提出生成的产物中可能还有FeO,请设计实验方案验证(用化学方法) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com