
【题目】《我在故宫修文物》展示了专家精湛的技艺和对传统文化的热爱与坚守,也令人体会到化学方法在文物保护中的巨大作用。某博物馆修复出土铁器的过程如下。
(1)检测锈蚀产物
主要成分的化学式 | |||
Fe3O4 | Fe2O3·H2O | FeO(OH) | FeOCl |
铁器在具有O2、________等环境中容易被腐蚀。
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ. Fe转化为Fe2+ 。
Ⅱ. Fe2+在自然环境中形成FeO(OH),该物质中铁元素的化合价为_______。
Ⅲ. FeO(OH)和Fe2+反应形成致密的Fe3O4保护层,Fe2+的作用是_______。
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
Ⅳ. Fe3O4保护层被氧化为FeO(OH),如此往复腐蚀。
![]() (将反应补充完整)___________
(将反应补充完整)___________
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:
将铁器浸没在盛有0.5 mol/L Na2SO3、0.5 mol/L NaOH溶液的容器中,缓慢加热至60~90℃。一段时间,取出器物,用NaOH溶液洗涤至无Cl-。
① 检测洗涤液中Cl-的方法是________。
② 脱氯反应:FeOCl + OH-=FeO(OH) + Cl-。离子反应的本质是离子浓度的减小,比较FeOCl 与FeO(OH)溶解度的大小:________。
③ Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是________。
【答案】 H2O(潮湿) +3 c 4Fe3O4+O2+6H2O=12FeO(OH) 取少量洗涤液于试管中,加入稀硝酸和硝酸银的混合液,若无白色沉淀产生说明无Cl- S(FeOCl)>S[FeO(OH)] SO32-+6FeO(OH)=SO42-+2Fe3O4+3H2O
【解析】(1)铁器在具有O2、H2O(潮湿)等环境中容易被腐蚀。(2)Ⅱ. 根据化合物中化合价代数和为0可知FeO(OH)中铁元素的化合价为+3。Ⅲ.反应中元素的化合价均不变化,所以Fe2+的作用是既不是氧化剂也不是还原剂,答案选c。Ⅳ. 1mol四氧化三铁中含有1mol亚铁离子,失去1mol电子,所以根据电子得失守恒和原子守恒可知反应的方程式为4Fe3O4+O2+6H2O=12FeO(OH);(3)①氯离子可以利用硝酸银溶液检验,所以检测洗涤液中Cl-的方法是取少量洗涤液于试管中,加入稀硝酸和硝酸银的混合液,若无白色沉淀产生说明无Cl-。②离子反应的本质是离子浓度的减小,这说明FeO(OH)更难溶,因此FeOCl的溶解度大于FeO(OH)的溶解度。③1mol四氧化三铁中含有1mol亚铁离子,亚硫酸钠的氧化产物是硫酸钠,根据电子得失守恒、原子守恒以及电荷守恒可知Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是SO32-+6FeO(OH)=SO42-+2Fe3O4+3H2O。


科目:高中化学 来源: 题型:
【题目】下列关于实验操作的说法正确的是
A.稀释浓硫酸时,将蒸馏水沿器壁缓慢注入浓硫酸中
B.过滤时,漏斗里液体的液面要高于滤纸边缘
C.蒸发过程中,蒸发皿中没有水时才能停止加热
D.点燃可燃性气体如H2、CO等时,先检验气体纯度后点燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Science 杂志在2017年春节发表了南京理工大学的论文,报道了世界上首个成功合成的五氮阴离子盐 (N5)6(H3O)3(NH4)4Cl(白色固体),这是全氮含能材料中里程碑式的突破。该盐可简略表示如下,下列分析不合理的是( )
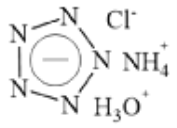
A. 五氮阴离子的化学式为 ![]() B. 该盐中氮元素的化合价均为-3价
B. 该盐中氮元素的化合价均为-3价
C. 该盐遇强碱能释放出NH3 D. 该盐中五氮阴离子具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证氯气的性质,某小组用如图所示的微型实验装置进行试验,a、b、c、d、e、是浸有相关溶液的滤纸.小组同学用KMnO4晶体与浓盐酸反应来制取少量的氯气,向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.其化学方程式为:KMnO4+HCl(浓)→KCl+Cl2↑+MnCl2+H2O (未配平),请回答下列问题: 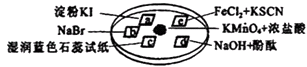
(1)上述反应中,元素的化合价升高;而元素被还原.
(2)配平上述反应: KMnO4+HCl(浓)═KCl+Cl2↑+MnCl2+H2O
(3)c处湿润蓝色石蕊试纸会先后 , 产生此现象的原因是: .
(4)e处滤纸的实验现象是: , 写出氯气与Fe2+反应的离子方程式是: .
(5)上述反应若在标准状况下产生56L的氯气,则转移电子为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个相同的密闭容器中分别充入CO2、H2、O2三种气体,当它们的温度和密度都相同,这三种气体的压强(p)从大到小的顺序是
A.p(H2)>p(CO2)>p(O2)B.p(H2)>p(O2)>p(CO2)
C.p(CO2)>p(H2)>p(O2)D.p(O2)>p(CO2)>p(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,满足表中图示物质在通常条件下一步转化关系的组合只有( )
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A.①②③
B.①③④
C.②③
D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)将4molN2和6molO2混合,所得气体在标准状况下的密度是_______g/L。
(2)有Na2SO4和Fe2(SO4)3的混合溶液中,已知其中c(Fe3+)=0.4mol/L,c(SO42-)=0.7mol/L,则此溶液中c(Na+)=_______mol/L。
(3)某普通酒精中乙醇的含量为97%,密度为0.90g/cm3,将乙醇看作溶剂,水看作溶质,该普通酒精中水的物质的量浓度是________ mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com