
A、B、C三种强电解质,它们在水中电离出的离子
如右表所示:
| 阳离子 | Ag+、Na+ |
| 阴离子 | NO3-、SO42-、Cl- |
下图Ⅰ所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27 g。常温下各烧杯中溶液的pH与电解时间t的关系如下图Ⅱ所示。据此回答下列问题:
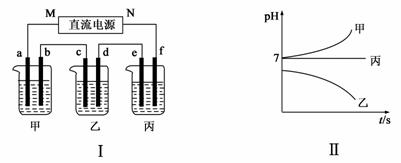
(1)M为电源的________(填“正”或“负”)极,A是________(填写化学式)。
(2)计算电极f上生成的气体在标准状况下的体积: 。
(3)写出b电极上发生的电极反应 ;
写出乙烧杯的电解池反应:_________________________________ 。
(4)要使丙恢复到原来的状态,应加入 g (填写化学式)。
科目:高中化学 来源: 题型:
公元前一世纪,我国已使用天然气,天然气的主要成分为甲烷。下列关于甲烷的叙述中,错误的是( )
A.通常情况下,甲烷跟强酸、强碱、强氧化剂不起反应
B.甲烷化学性质比较稳定,不能被任何氧化剂氧化
C.甲烷跟氯气反应无论生成CH3Cl、CH2Cl2、CHCl3还是CCl4,都属于取代反应
D.甲烷的四种取代物都难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家预测原子序数为114的元素具有相当稳定的同位素,它的位置在第7周期ⅣA族,称为类铅。下列关于它的性质的叙述中,错误的是( )
A.它的最外层电子数为4
B.它的金属性比铅强
C.它具有7个电子层
D.它的最高价氧化物的水化物是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列依据热化学方程式得出的结论正确的是( )
A.若2H2(g)+O2(g) ===2H2O(g) ΔH=-483.6 kJ·mol-1,则1 mol H2 燃烧放出热量
为241.8 kJ·mol-1
B.若C(石墨,s) ===C(金刚石,s) ΔH > 0,则石墨比金刚石稳定
C.已知NaOH(aq)+HCl(aq )===NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,
)===NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,
则20.0g NaOH 固体与稀盐酸完全中和,放出28.7 kJ的热量
固体与稀盐酸完全中和,放出28.7 kJ的热量
D. 已知2C(s)+2O2(g) ===2CO2(g) ΔH1;2C(s)+O2(g) =2CO(g) ΔH2,则ΔH1>ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:
电池:Pb(s) + PbO2(s) + 2H2SO4(aq) = 2PbSO4(s) + 2H2O(l)
电解池: 2Al + 3H2O = Al2O3 + 3H2↑,对该电解过程,以下判断正确的是( )
| 电 池 | 电 解 池 | |
| A | H+ 移向Pb电极 | H+ 移向Pb电极 |
| B | 每消耗3mol Pb | 生成1mol Al2O3 |
| C | 正极:PbO2+4H++2e-=Pb2++2H2O | 阳极:2Al+3H2O-6e-=Al2O3+6H+ |
| D | Pb电极反应质量不变 | Pb电极反应质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应,产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是
①金属钠在纯氧中燃烧 ②FeSO4溶液中滴入NaOH溶液并在空气中放置一段时间后 ③FeCl3溶液中滴入KSCN溶液 ④无水硫酸铜放入医用酒精中
A.③②①④ B.②③①④ C.③①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
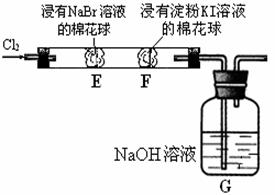
某化学小组用下图所示装置验证卤素单质氧化性的相对强弱。下列说法不正确的是
A.E处棉花球变成黄色,说明Cl2的氧化性比Br2强
B.F处棉花球变成蓝色,说明Br2的氧化性比I2强
C.E处发生反应的离子方程式为:Cl2+ 2Br- = 2Cl- + Br2
D.G装置中NaOH溶液与Cl2反应的离子方程式为:
Cl2 + 2OH- = ClO- + Cl- + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在1~18号元素中(除稀有气体元素)用元素符号或化学式填写:
(1)简单离子中,半径最小的是________。
(2)原子半径最小的是________,原子半径最大的是________。
(3)与水反应最剧烈的金属单质是________。
(4)最高价氧化物的水化物中,酸性最强的是________,碱性最强的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| 化学式 | 电离常数 |
| HClO | Ka=3×10-18 |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 |
A.c(HCO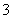 )>c(ClO-)>c(OH-)
)>c(ClO-)>c(OH-)
B.c(ClO-)>c(HCO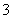 )>c(H+)
)>c(H+)
C.c(HClO)+c(ClO-)=c(HCO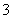 )+c(H2CO3)
)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO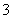 )+c(ClO-)+c(OH-)
)+c(ClO-)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com