(2013?黄山一模)铁及其化合物在生产和生活中有着广泛的应用.
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:
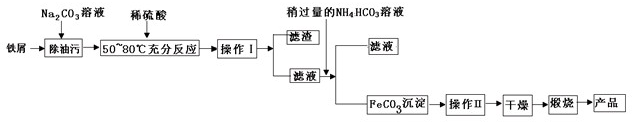
回答下列问题:
①操作Ⅰ、Ⅱ的名称分别是
过滤
过滤
、
洗涤
洗涤
.
②写出在空气中煅烧FeCO
3的化学方程式
4FeCO3+O2=2Fe2O3+4CO2
4FeCO3+O2=2Fe2O3+4CO2
;
③.煅烧如果不充分,产品中将有Fe
2+ 存在,试设计实验检验产品中有无Fe
2+.
(2)有些同学认为KMnO
4溶液滴定也能进行铁元素含量的测定.
a.称取2.850g绿矾(FeSO
4?7H
2O)产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO
4溶液滴定至终点,消耗KMnO
4溶液体积的平均值为20.00mL.
①写出酸性KMnO
4溶液与FeSO
4溶液反应的离子方程式
MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O
MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O
②计算上述样品中FeSO
4?7H
2O的质量分数为
97.5%
97.5%
已知M(FeSO
4?7H
2O)=278g/mol]
③滴定达到终点时锥形瓶中溶液颜色变化为
紫红色
紫红色
④下列操作会导致样品中FeSO
4?7H
2O的质量分数的测定结果偏高的有
b
b
.
a.未干燥锥形瓶
b.盛装标准液的滴定管没有用标准液润洗
c. 滴定终点时滴定管尖嘴中产生气泡
d.量取待测液,视线注视刻度时开始平视、结束俯视.




 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案