
 ,结构式是:
,结构式是: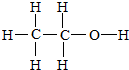 、结构简式是:CH3CH2OH或C2H5OH、分子式是:C2H6O,乙醇分子中官能团是羟基.
、结构简式是:CH3CH2OH或C2H5OH、分子式是:C2H6O,乙醇分子中官能团是羟基.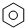 表示苯分子结构式,故答案为:
表示苯分子结构式,故答案为: ;
; ,结构简式是:CH3CH2OH或C2H5OH、乙醇分子中官能团是羟基(-OH)、
,结构简式是:CH3CH2OH或C2H5OH、乙醇分子中官能团是羟基(-OH)、 ,CH3CH2OH或C2H5OH;-OH;羟基.
,CH3CH2OH或C2H5OH;-OH;羟基.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、配位化合物中必定存在配位键 |
| B、配位键仅存在于配位化合物中 |
| C、[Cu(H2O)4]2+中的Cu2+提供空轨道,H2O中的氧原子提供孤对电子形成配位键 |
| D、配位化合物在半导体等尖端技术、医学科学、催化反应和材料化学等领域都有着广泛的应用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH3经催化氧化生成NO |
| B、N2和O2在一定条件下合成NO |
| C、NO与O2反应生成NO2 |
| D、由NH3制碳酸氢铵 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:
 若将有机物分子中碳、氢元素符号省略,而只表示分子中键的连接情况,每个拐点或终点均表示一个碳原子,称为键线式,如丙烷的键线式为.人体对维生素的需要量虽少,但一旦缺乏,人体就不能正常发育,还会引起疾病,下面是维生素A的结构简式:
若将有机物分子中碳、氢元素符号省略,而只表示分子中键的连接情况,每个拐点或终点均表示一个碳原子,称为键线式,如丙烷的键线式为.人体对维生素的需要量虽少,但一旦缺乏,人体就不能正常发育,还会引起疾病,下面是维生素A的结构简式:查看答案和解析>>
科目:高中化学 来源: 题型:
| 键能 | 键能 | 键能 | 键能 | ||||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 431 | H-O | 464 |
| S═S | 255 | H-S | 339 | C-F | 427 | C-O | 347 |
| C-Cl | 330 | C-I | 218 | H-F | 565 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 在常温常压下,可利用下列装置来测定气体体积,抽气装置E用以调节装置中的气压差,减小实验误差.
在常温常压下,可利用下列装置来测定气体体积,抽气装置E用以调节装置中的气压差,减小实验误差.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、周期表中的主族都有非金属元素 |
| B、周期表中的主族都有金属元素 |
| C、周期表中的非金属元素都位于短周期 |
| D、周期表中的过渡元素都是金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com