
科目:高中化学 来源: 题型:
下列各组在溶液中的反应,不管反应物的量是多少,都能用同一离子方程式表示的是( )
A、FeBr2与Cl2
B、Ba(OH)2与H2SO4
C、HCl与Na2CO3
D、NaHCO3与Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化不能说明发生了化学变化的是
A. 变化时有电子的得失或共用电子对的形成
B. 变化过程中有旧化学键的断裂和新化学键形成
C. 变化前后原子的种类和数目没有改变,分子种类增加了
D. 变化时释放出能量
查看答案和解析>>
科目:高中化学 来源: 题型:
现有一部分氧化的Na2SO3样品ag,为了测定其中Na2SO3的质量分数,设计了如下方案,其中明显不合理的是
A. 将样品配制成溶液V1L,取其中25.00 mL用标准KMnO4溶液滴定,消耗标准KMnO4溶液V2 mL
B. 向样品中加足量H2O2,再加足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为b g
C. 将样品与足量稀盐酸充分反应后,再加入足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为c g
D. 将样品与足量稀盐酸充分反应,生成的气体依次通过盛有饱和NaHSO3的洗气瓶、盛有浓H2SO4的洗气瓶、盛有碱石灰的干燥管Ⅰ、盛有碱石灰的干燥管Ⅱ,测定干燥管Ⅰ增重d g
查看答案和解析>>
科目:高中化学 来源: 题型:
高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
查阅资料:①MnCO3难溶于水,潮湿时易被空气氧化,100℃开始分解。
②Mn(OH)2开始沉淀时pH=7.7。
实验过程:
Ⅰ. 用图1所示装置制备MnSO4溶液。
Ⅱ. 边搅拌边向MnSO4溶液中加入稍过量NaHCO3溶液,过滤。
Ⅲ. 洗涤沉淀。
Ⅳ. 洗涤后的沉淀在温度低于100℃的条件下干燥,制得高纯MnCO3固体。
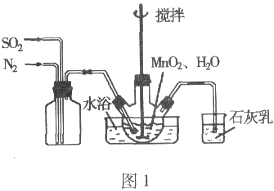
(1)图1中石灰乳的作用是__________,烧瓶中发生反应的化学方程式是__________。
(2)根据图2“浸锰”的反应适宜时间是____________________。若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如图3。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是______________________________。

图2 图3
(3)Ⅱ中加入稍过量NaHCO3溶液,控制溶液pH在__________范围,写出加入NaHCO3,后发生反应的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知气体的摩尔质量越小,扩散速度越快。如图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正确的是( )

A、甲是浓氨水,乙是浓硫酸
B、甲是浓盐酸,乙是浓氨水
C、甲是浓氨水,乙是浓盐酸
D、甲是浓硝酸,乙是浓氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
有关氨气的实验较多,下面对这些实验原理的分析中,正确的是( )
A、氨气极易溶于水,可以用来做喷泉实验
B、氨气的还原性可以解释氨气与氯化氢的反应实验
C、NH3·H2O不稳定,实验室可用NH4Cl和石灰水制取氨气
D、NH3液化时放出大量的热,因而,不能用氨作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关铝及其化合物的叙述正确的是( )
A.铝粉与三氧化钨共热可制取金属钨
B.足量铝分别与含1 mol HCl、1 mol NaOH的溶液反应,产生相同量的氢气
C.工业上用电解熔融Al2O3的方法冶炼铝
D.在浓硝酸中加入等体积的浓硫酸后,立即加入铝片,铝片表面发生钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸是二元弱酸,草酸氢钾溶液呈酸性。在0.1mol·L-1 KHC2O4溶液中,下列关系正确的是 ( )
A.c(K+)+c(H+) = c(HC2O4-)+c(OH-)+c(C2O42-)
B.c(HC2O4-)+c (C2O42-) = 0.1 mol·L-1
C.c(C2O42-) < c(H2C2O4)
D.c(K+) = c(H2C2O4)+c(HC2O4-)+c(C2O42-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com