
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在Al2(SO4)3和MgSO4组成的混合物中,Al3 +与Mg2+的物质的量之比为2
+与Mg2+的物质的量之比为2 ∶3,则在含有2 mol SO
∶3,则在含有2 mol SO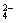 的混合物中,MgSO4的质量是多少克?
的混合物中,MgSO4的质量是多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的 pH 在 5.0~6.0 之间,通过电解生成 Fe(OH)3 沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成 浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示: (1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,则无法使悬浮物形成浮渣。
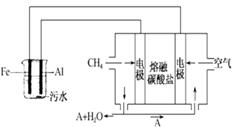

此时,应向污水中加入适量的_________。
a. H2SO4 b.BaSO4 c.Na2SO4 d.NaOH e.CH3CH2OH
(2)电解池阳极的电极反应分别是①______________;
②4OH--4e-=2H2O+O2↑
(3)电极反应①和②的生成物反应得到 Fe(OH)3 沉淀的离子方程式是__________。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以 CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应是 CH4+4CO2-8e-===5CO2+2H2O。
①正极的电极反应是______________。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。 则 A 物质的化学式是___________。
(5)实验过程中,若在阴极产生了 44.8L(标准状况)气体,则熔融盐燃料电池消耗 CH4_____L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
设计实验证明酸性强弱顺序:HCl>H2CO3>H2SiO3。
(1)写出实验原理的化学反应方程式________________。
(2)设计本实验所依据的化学原理是________________。
(3)实验中必须用到的药品有________________,所需的实验仪器有________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NaHSO4在水溶液中能够电离出H+、Na+、SO42- 。下列对于NaHSO4的分类中不正确的是( )
A、NaHSO4是盐 B、NaHSO4是酸
C、NaHSO4是钠盐 D、NaHSO4是酸式盐
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)将碳酸钙、稀盐酸、铁、氧气四种物质填写到下图的适当位置。

(2)从(1)中的四种物质中选出一种或几种为反应物,按下述反应类型,各写一个化学方程式。
①分解反应:__________________________________________。
②化合反应:__________________________________________。
③置换反应:__________________________________________。
④复分解反应:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。
B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。
C.氨气分子是极性分子而甲烷是非极性分子。
D.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量Ca2+、Mg2+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
 |
提供的试剂:
饱和Na2CO3溶液、 饱和K2CO3溶液 、NaOH溶液 、BaCl2溶液、Ba(NO3)2溶液
(1)欲除去溶液I中的Ca2+、Mg2+、SO42-离子,选出A所代表的试剂,按滴加顺序依次为 _______________________________________(只填化学式)。
(2)操作Ⅲ的名称是_________,所需用到的仪器主要有铁架台、酒精灯、铁圈、______________________ (填仪器名称)。
(3)加盐酸的目的是(用离子方程式表示) 、 。
Ⅱ.一份无色溶液中可能含有Na+ 、Fe3+、H+ 、Mg2+、CO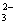 、OH-、HCO
、OH-、HCO 、Cl-、SO42-等离子中的若干种。为了确定溶液的组成,进行了如下操作:
、Cl-、SO42-等离子中的若干种。为了确定溶液的组成,进行了如下操作:
① 向溶液中滴加酚酞试液,溶液显红色;
② 取2 mL溶液,先加足量稀硝酸酸化,有气体产生,再加氯化钡溶液进行检验,没有明显现象;
(4)原溶液中一定存在的离子是 , 一定不存在的离子是 。
(5)经过上述操作后,还不能肯定是否存在的离子是 。对可能含有的离子,如何进行实验以进一步检验。 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com