
在10L 恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
| 实验 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
下列说法正确的是( )
A.实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率v(N)=1.0×10-2mol/(L·min)
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡时,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
科目:高中化学 来源: 题型:
已知:① 2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1 ②H2(g)+S(g)=== H2S(g) ΔH=-20.1 kJ·mol-1。
下列判断正确的是( )
A.1 mol氢气完全燃烧生成液态水吸收热量241.8 kJ
B.1 mol H2O(g)和1 mol H2S(g)的能量相差221.7 kJ
C.由①②知,水的热稳定性小于硫化氢
D.若反应②中改用固态硫,1 mol S(s)完全反应,放出的热量小于20.1 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1︰1︰1时,实际参加反应的FeS与HNO3的物质的量之比为( )
A.1∶6 B.1∶7 C.2∶11 D.16∶25
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是( )
A.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
B.N2(g)+3H2(g) 2NH3(g) △H<0,其他条件不变时升高温度,反应速率v (H2)和氢气的平衡转化率均增大
2NH3(g) △H<0,其他条件不变时升高温度,反应速率v (H2)和氢气的平衡转化率均增大
C.升高温度通过降低活化能而加快化学反应速率
D.常温下,反应C(s)+CO2(g) === 2CO(g)不能自发进行,则该反应的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验不能达到实验目的的是( )
①实验窒用无水乙醇和浓硫酸共热到140℃即可制取乙烯
②验证R—X是碘代烷,把R—X与NaOH水溶液混合加热,再往其中加入硝酸银溶液即可
③做醛的还原性实验,向乙醛溶液中加入新制的Cu(OH)2悬浊液即可得到红色沉淀
④检验淀粉已水解,将淀粉与水和稀硫酸加热一段时间后,加入银氨溶液即可
⑤实验室制备乙酸乙酯,把乙醇和乙酸及稀硫酸溶液共热即可
A.①②③④⑤ B.①③④ C.①②③⑤ D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中,与100 mL 0.5 mol/L NaCl溶液所含的Cl- 物质的量浓度相同的是
A.100 mL 0.5 mol/L MgCl2溶液 B.200 mL 0.25 mol/L AlCl3溶液
C.50 ml 1 mol/L NaCl溶液 D.50 ml 0.5 mol/L HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求填空:
(1)2.7 g H2O所含氢原子数与 ▲ L(标准状况下)NH3所含氢原子数相等。
(2)以下物质:① NH3 ② CaCO3 ③ 蔗糖 ④ 饱和食盐水 ⑤ H2SO4 ⑥ Cu
属于电解质的有 ▲ (填序号)。
(3)用单线桥标出下列反应中电子转移的方向和数目:
MnO2+4HCl(浓) 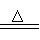 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
① 该反应中的氧化剂是 ▲ 。
②如反应中转移了0.2 mol电子,则产生的Cl2在标准状况下体积为 ▲ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
在1.0 L密闭容器中放入0.10 mol A (g),在一定温度进行如下反应:A(g)B(g)+C(g) ΔH=+85.1 kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p /100 kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为________。
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为________________________________________________________________________,
平衡时A的转化率为________,列式并计算反应的平衡常数K_______________。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总=________mol,n(A)=________mol。
②下表为反应物A浓度与反应时间的数据,计算a=__________________。
| 反应时间t/h | 0 | 4 | 8 | 16 |
| c(A)/(mol·L-1) | 0.10 | a | 0.026 | 0.006 5 |
分析该反应中反应物的浓度c(A)变化与时间间隔(Δt)的规律,得出的结论是________,由此规律推出反应在12 h时反应物的浓度c(A)为________mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com