
下列说法中不正确的是( )
A.乙烯与苯都能使溴水褪色,但褪色原理不同
B. 1 mol乙烯与Cl2完全加成,然后与Cl2发生取代反应,共消耗氯气 5mol
C.溴水遇到乙醛溶液出现褪色现象,是因为发生了氧化反应
D.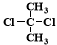 与
与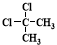 互为同分异构体
互为同分异构体
科目:高中化学 来源:2015-2016学年陕西省高一5月月考化学试卷(解析版) 题型:选择题
下列关于苯的说法中,正确的是( )
A. 苯不能使酸性KMnO4溶液退色,属于饱和烃
B. 常温下苯是一种易溶于水且密度比水小的液体
C. 苯不具有典型的双键,故苯不能发生加成反应
D. 苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高一下第二阶段考试化学试卷(解析版) 题型:填空题
A、B、C、D、E、 F是周期表中短周期的六种元素,有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 地壳中含量最多的元素 |
B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
E | E与D同周期,且在该周期中原子半径最小 |
F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
(1)请写出B、D、F三种元素的名称: 、 、 。
(2)A与C以原子个数比为1:1形成的化合物的电子式为 ,
将4mol该化合物投入到2L1mol/L BE3溶液中的离子方程式
为 、 。
(3)写出实验室制备F的氢化物的化学方程式 。
(4)下图可用于实验证明D、E的非金属性的强弱。
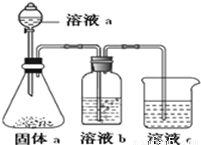
①溶液a和b分别为 , (写化学式)。
②非金属性D E(填大于或小于),请从原子结构的角度解释原因: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高一下第二阶段考试化学试卷(解析版) 题型:选择题
化学与环境、材料、信息、能源关系密切,下列说法正确的是 ( )
A.绿色化学的核心是应用化学原理对环境污染进行治理
B.开发高效氢能、太阳能等新型电动汽车,以解决城市机动车尾气排放问题
C.PM 2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体
D.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下第二阶段考试化学试卷(解析版) 题型:选择题
有8种物质:① 乙烷;② 乙烯;③ 乙炔;④ 苯;⑤ 甲苯;⑥ 溴乙烷;⑦ 聚丙烯;⑧ 环己烯。其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )
A.①②③⑤ B.④⑥⑦⑧ C.①④⑥⑦ D.②③⑤⑧
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下第二阶段考试化学试卷(解析版) 题型:选择题
下列系统命名法正确的是( )
A. 2-甲基-4-乙基戊烷
B. 2,3-二乙基-1-戊烯
C.2-甲基-3-丁炔
D.对二甲苯
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省协作体高二下学期第一次联考化学试卷(解析版) 题型:填空题
氨在国民经济中占有重要地位。
(1)NH3的电子式为
(2)实验室中制取氨气的化学方程式为 ,生成的气体可以用蘸有浓盐酸的玻璃棒来检验,将产物溶于水,溶液呈酸性,用离子方程式表示原因 ;
溶液中离子浓度由大到小的顺序为
(3)欲快速制取氨气,可将浓氨水滴入固体氢氧化钠中,其装置如图,请结合化学用语从化学平衡的角度解释:
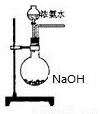
(4)将SO2气体通入氯化钡溶液,未见有沉淀生成,继续通入NH3,则出现白色沉淀,请写出反应的离子方程式 ;若将SO2气体通入酸化的硝酸钡溶液,也产生白色沉淀,用离子方程式加以说明 。
(5)氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。
肼——空气燃料电池是一种碱性电池,该电池放电时,负极的反应式 。
(6)氮氧化物的排放会对空气造成污染,利用氧化法除去烟气中的氮氧化物。首先向氮氧化物中补充氧气,然后将混合气体通入石灰乳中,使之转化为硝酸钙。已知某氮氧化物由NO和NO2组成,且n(NO):n(NO2)=1:3.写出氧化吸收法除去氮氧化物的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高一下学科竞赛化学试卷(解析版) 题型:实验题
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
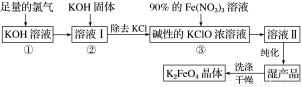
请回答下列问题:
(1)写出向KOH溶液中通入足量Cl2发生反应的离子方程式:________________________。
(2)在溶液Ⅰ中加入KOH固体的目的是____________(填字母)。
A.为下一步反应提供碱性的环境
B.使KClO3转化为KClO
C.与溶液Ⅰ中过量的Cl2继续反应,生成更多的KClO
D.KOH固体溶解时会放出较多的热量,有利于提高反应速率
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为___________________________________________________。每制得59.4 g K2FeO4,理论上消耗氧化剂的物质的量为________ mol。
(4)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:______ FeO42-+______ H2O===______ Fe(OH)3(胶体)+______ O2↑+______ OH-。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一下十一次联考化学试卷(解析版) 题型:选择题
我国东海发现大型油田。下列关于石油的说法中正确的是
A、石油属于可再生矿物能源
B、石油主要含有碳、氢两种元素
C、石油的裂化是物理变化
D、石油分馏的各馏分均是纯净物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com