


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
| A、标准状况下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
| B、常温下,2.3g Na完全与O2反应失去的电子数为0.1NA |
| C、100mL 18.4mol?L-1的硫酸与足量铜反应,生成二氧化硫的分子数小于0.92 NA |
| D、在密闭容器中加入1.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
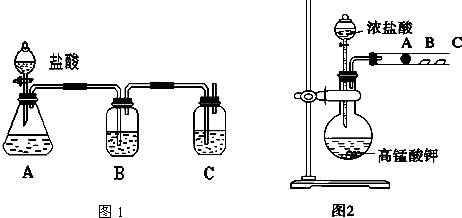
查看答案和解析>>
科目:高中化学 来源: 题型:
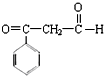 是一种重要的化工原料.A、B、C、D、E之间的转化关系如图:
是一种重要的化工原料.A、B、C、D、E之间的转化关系如图: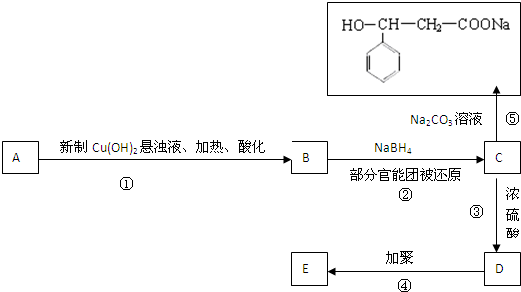
查看答案和解析>>
科目:高中化学 来源: 题型:
 某兴趣小组同学进行乙醛的银镜反应实验的操作步骤如下:
某兴趣小组同学进行乙醛的银镜反应实验的操作步骤如下:| 实验变量 实验序号 | 银氨溶液的量/mL | 乙醛的量/滴 | 温度/℃ | 反应混合液的pH | 出现银镜的时间/min |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
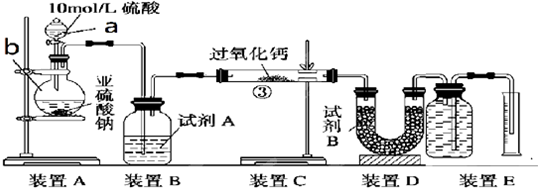
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该烷烃的物质的量为(b-a)mol |
| B、该烷烃的物质的量为a mol |
| C、该烷烃的物质的量为(b-a)/2 mol |
| D、不能求出该烷烃的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子序数由大到小的顺序是C>A>B |
| B、原子半径由大到小的顺序是r(B)>r(A)>r(C) |
| C、离子半径由大到小的顺序是r(C-)>r(B2+)>r(A2-) |
| D、原子最外层电子数由多到少的顺序是B>A>C |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com