
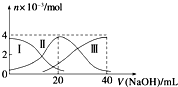
 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )| A. | 当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) | |
| B. | 等浓度的NaOH溶液与H2A溶液按2:1混合后,其溶液中水的电离程度比纯水大 | |
| C. | NaHA溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A) | |
| D. | 向上述加入20 mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少 |
分析 A.根据图象知,当V(NaOH)=20时,发生反应为NaOH+H2A═NaHA+H2O,溶液主要为NaHA,电离为主,溶液显酸性;
B.酸或碱抑制水电离,含有弱根离子的盐促进水电离;
C.根据物料守恒和电荷守恒判断;
D.二者恰好反应生成NaHA,加水稀释HA-电离和水解.
解答 解:A.根据图象知,当V(NaOH)=20 mL时,发生反应为NaOH+H2A═NaHA+H2O,溶质主要为NaHA,HA-电离程度大于水解程度,溶液显酸性,水和HA-都电离出氢离子,只有HA-电离出A2-,所以离子浓度大小顺序是c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),故A错误;
B.等浓度的NaOH溶液与H2A溶液按体积2:1混合后,二者恰好反应生成Na2A和水,Na2A是强碱弱酸盐促进水电离,故B正确;
C.根据电荷守恒得c(OH-)+2c(A2-)+c(HA-)=c(H+)+c(Na+),根据物料守恒得c(Na+)=c(HA-)+c(H2A)+c(A2-),所以得c(OH-)+c(A2-)=c(H+)+c(H2A),故C错误;
D.二者恰好反应生成NaHA,加水稀释HA-电离和水解,但氢氧根离子浓度减小,但水解程度大于电离程度,所以pH增大,故D错误;
故选:B.
点评 本题考查酸碱混合溶液定性判断,明确图象中酸碱混合时溶液中的溶质是解答本题的关键,抓住图象进行分析即可,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 是银白色、质软的金属 | B. | 能形成+3价的化合物 | ||
| C. | Tl的金属性强于铝 | D. | 能与硝酸反应放出H2并生成硝酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的空间构型是正四面体,所以CH2Cl2有两种不同的结构 | |
| B. | 含有C、H元素的物质就是有机物,所有的有机物都可以燃烧 | |
| C. | 任何烷烃分子都不可能为平面结构 | |
| D. | 易溶于汽油、酒精、苯等有机溶剂的物质都是有机化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14N与15N具有相同的质子数 | B. | 18O和17O具有相同的电子数 | ||
| C. | 18O和19F具有相同的中子数 | D. | 12C与13C具有相同的质量数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ②③ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
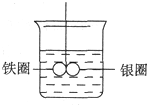 如图所示,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡.小心地从烧杯中央滴入CuSO4溶液.
如图所示,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡.小心地从烧杯中央滴入CuSO4溶液.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
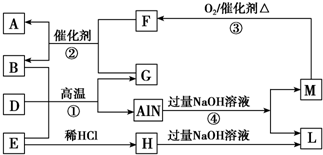
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙烷(乙烯):酸性KMnO4溶液洗气 | B. | 乙醇(乙酸):生石灰蒸馏 | ||
| C. | 乙酸乙酯(乙醇):水分液 | D. | 溴苯(溴):CCl4溶液萃取分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com