
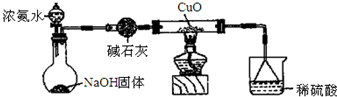
分析 浓氨水逐滴加入到氢氧化钠固体可以制取氨气,氨气为碱性气体应选择碱性干燥剂碱石灰干燥,氨气具有还原性,与氧化铜发生还原反应生成氮气和铜、水,为防止过量氨气污染空气,可用稀硫酸吸收氨气,据此解答.
(1)为防止水蒸气使加热试管受热不均匀,所以需对含有水蒸气的氨气进行干燥,硫酸和氨气反应,防止倒吸,用倒扣漏斗;
(2)根据温度对气体溶解度的影响以及平衡移动原理来分析;
(3)根据硬质玻璃管中发生的反应2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O分析;
(4)常温下,若氨水与稀硫酸恰好完全中和,生成硫酸铵溶液,铵根离子部分水解,溶液显酸性,据此比较各离子浓度的大小.
解答 解:(1)制取的氨气中含有水蒸气,氨气与氧化铜反应需要加热,所以氨气进入硬质试管前应进行干燥,所以碱石灰作用为干燥氨气,氨气极易溶于硫酸,倒扣的漏斗球形部分空间大,可防止倒吸,
故答案为:吸收水蒸气;防止倒吸;
(2)氧化钙与水反应放出热量,使氨气在水中溶解度降低而逸出,溶液中氢氧根离子浓度增大,使平衡NH3+H2O?NH3•H2O?NH4++OH-,逆向移动,有利于氨气逸出,
故答案为:NaOH吸水放热,使溶液温度升高,有利于NH3•H2O分解;c(OH-)增大,使NH3+H2O?NH4++OH-平衡左移,也有利于氨气的逸出;
(3)硬质玻璃管中发生的反应2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O,氧化铜为黑色、铜为红色,所以可观察到的实验现象是黑色粉末变为红色,有无色液滴产生,
故答案为:黑色粉末变为红色,有无色液滴产生;
(4)1mol硫酸铵,含有2mol铵根离子,1mol硫酸根离子,铵根离子部分水解,则溶液显示酸性:c(H+)>c(OH-),铵根离子水解程度较小、硫酸根离子不水解,则c (NH4+)>c(SO42-)>c(H+),则溶液中各离子的浓度由大到小的顺序为:c (NH4+)>c(SO42-)>c(H+)>c(OH-),
故答案为:(NH+4)>c(SO42-)>c(H+)>c(OH-).
点评 本题主要考查了氨气具有还原性实验探究、化学平衡移动原理等知识,题目难度不大,注意硫酸铵混合溶液中离子浓度的大小比较,为易错点.


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 假设 | B. | 实验 | C. | 做结论 | D. | 观察 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定浓度的氨水加水稀释的过程中,c(NH4+)/c(NH3•H2O)的比值减小 | |
| B. | pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)>c(CH3COO -) | |
| C. | 常温下0.4mol/LHB溶液和0.2mol/LNaOH溶液等体积混合后溶液的pH=3,则溶液中微粒浓度存在下面关系:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) | |
| D. | c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c(NH4)2SO4>c(NH4Cl) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 45mL | B. | 180mL | C. | 90mL | D. | 135mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
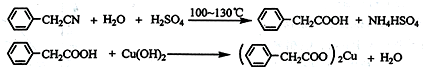
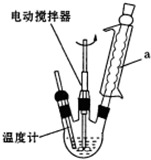
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
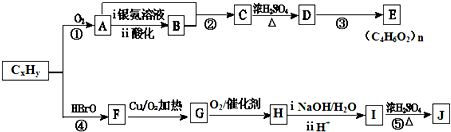


 +2H2O.
+2H2O.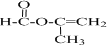 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com