
| A. | 凡是能导电的物质都是电解质 | |
| B. | 凡是不能导电的物质一定是非电解质 | |
| C. | 电解质溶液能导电的原因是溶液中存在自由移动的离子 | |
| D. | 盐酸能导电的原因是溶液在电流作用下电离成了自由移动的离子的缘故 |
分析 A、电解质是在水溶液或是熔融状态下能导电的化合物;
B、非电解质是在水溶液或是熔融状态下都不能导电的化合物;
C、电解质溶液能导电的原因是溶液中存在自由移动的离子;
D、电离是不需要外加电源的电流而离解出自由移动离子的过程.
解答 解:A.电解质一定属于化合物,如金属铜能导电,但是不属于电解质,故A错误;
B.电解质不一定都能导电,如氯化钠固体不导电,不能导电的物质不一定是非电解质,故B错误;
C.解质溶液能导电的原因是溶液中存在自由移动的离子,能和发生定向移动,故C正确;
D.电解质溶于水或熔化下能电离,通电时离子作定向移动,电离出离子的过程不需要电流,故D错误.
故选C.
点评 本题考查电解质的导电及电解质的判断,明确电解质为化合物及电解质电离的条件即可解答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 化学平衡状态是反应的最大限度,此时反应停止了 | |
| B. | 水通电时能分解成氢气和氧气,氢气和氧气点燃能生成水,这两个反应是可逆反应 | |
| C. | 可逆反应的化学方程式中,用可逆号代替等号 | |
| D. | 当温度或浓度改变时,原来的化学平衡一定不被破坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
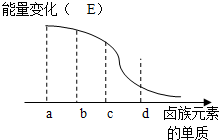 A、B、C、D为按顺序排列的前四种卤素单质,仔细分析下表中的数据,回答有关问题.
A、B、C、D为按顺序排列的前四种卤素单质,仔细分析下表中的数据,回答有关问题.| 卤素单质 | 密度(标准状况下) | 沸点/℃ | 熔点/℃ | 溶解度(标准状况下,100g水中) |
| A | 1.696 g•l-1 | -188.1 | -219.6 | -- |
| B | 3.214 g•l-1 | -34.6 | -101 | 226 cm3 |
| C | 3.119 g•cm-3 | 58.78 | -7.2 | 4.16 g |
| D | 4.93 g•cm-3 | 184.4 | 113.5 | 0.029 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠在氯气中燃烧,有白雾生成 | |
| B. | 铜在氯气中燃烧,生成蓝色的氯化铜颗粒 | |
| C. | 钠投入硫酸铜溶液中,会产生蓝色沉淀 | |
| D. | 钠在空气中燃烧后得到白色粉末状固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该该反应是氧化还原反应 | B. | 钾元素化合价降低 | ||
| C. | 铁元素化合价不变 | D. | 反应是置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32 g | B. | 33 g | C. | 33 g•molˉ1 | D. | 32 g•molˉ1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com