
Ⅰ.某兴趣小组用如图装置做了两次实验。
实验①:向甲池的Pt电极表面通氢气,发现电流计指针发生了偏转,乙池的Pt电极表面出现气泡。
实验②:向乙池的Pt电极表面通氧气,发现电流计指针也发生了偏转,且偏转方向与实验①相同,同时甲池的Pt电极表面也出现气泡。

(1)实验①,甲池通氢气的Pt电极为________极,电极反应式为__________________________。
(2)实验②,乙池通氧气的Pt电极为________极,电极反应式为__________________________。
(3)两次实验中原电池的总反应相同,总反应的离子方程式为________________________________。
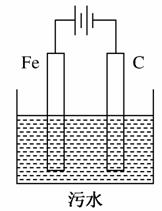
Ⅱ.电解 池污水处理技术已很成熟。富含悬浮物的工业污水采用如图装置进行处理:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,吸附部分悬浮物沉降,同时阴极产生的气泡将部分悬浮物带到水面形成浮渣层,然后滤去沉淀撇掉浮渣层。富含有机废物的生活污水也可用同样方法进行处理。污水中的有机废物能被阳极的某一产物迅速降解成二氧化碳、水等无机物。
池污水处理技术已很成熟。富含悬浮物的工业污水采用如图装置进行处理:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,吸附部分悬浮物沉降,同时阴极产生的气泡将部分悬浮物带到水面形成浮渣层,然后滤去沉淀撇掉浮渣层。富含有机废物的生活污水也可用同样方法进行处理。污水中的有机废物能被阳极的某一产物迅速降解成二氧化碳、水等无机物。
(1)电解处理过程中,若污水中离子浓度较小,导电能力较差,处理效率下降,此时可向污水中加入适量的________(填选项字母)。
A.BaSO4 B.CH3COOH
C.NaNO3 D.CH3OH
(2)电解处理过程中,阳极实际发生了两个电极反应,阳极的电极反应式分别是①______________________________;②__________________________。
解析 Ⅰ.(1)实验①中,通氢气的一极为负极,在碱性条件下,电极反应方程式为H2+2OH--2e-===2H2O。(2)实验②中,通氧气的一极为正极,在酸性条件下,电极反应方程式为O2+4H ++4e-===2H2O。(3)两次实验中原电池的总反应相同,总反应的离子方程式为H++OH-===H2O。Ⅱ.(1)要增强溶液的导电能力,但不能使电极反应发生改变,故加入溶于水的强电解质,如题中的NaNO3,即选C。(2)电解过程中,铁为阳极,铁先失去电子,Fe-2e-===Fe2+,同时,还会发生:2H2O-4e-===4H++O2↑。
++4e-===2H2O。(3)两次实验中原电池的总反应相同,总反应的离子方程式为H++OH-===H2O。Ⅱ.(1)要增强溶液的导电能力,但不能使电极反应发生改变,故加入溶于水的强电解质,如题中的NaNO3,即选C。(2)电解过程中,铁为阳极,铁先失去电子,Fe-2e-===Fe2+,同时,还会发生:2H2O-4e-===4H++O2↑。
答案 Ⅰ.(1)负 H2-2e-+2OH-===2H2O (2)正 O2+4e-+4H+===2H2O (3)H++OH-===H2O
Ⅱ.(1)C (2)①Fe-2e-===Fe2+ ②2H2O-4e-===O2↑+4H+


科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.1 mol氦气中有2NA个氦原子
B.14 g氮气中含NA个氮原子
C.2 L 0.3 mol·L-1 Na2SO4溶液中含0.6 NA个Na+
D.18 g水中所含的电子数为8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO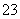 、NO
、NO 、SO
、SO 、SiO
、SiO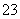 。现进行如下实验:
。现进行如下实验:
Ⅰ.取少量溶液,加入KSCN溶液,无明显变化。
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅲ.向Ⅱ中所得的溶液中加入BaCl2溶液,有白色沉 淀生成。
淀生成。
Ⅳ.向Ⅱ中所 得的溶液中加入过量浓氨水,仅有红褐色沉淀生成。过滤,在所得溶液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成。
得的溶液中加入过量浓氨水,仅有红褐色沉淀生成。过滤,在所得溶液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成。
请回答下列问题:
(1)该废水一定含有的离子是________。
(2)实验Ⅱ中加入少量盐酸生成无色气体的离子方程式是___________。
(3)过滤除去Ⅳ中的蓝色沉淀,调整滤液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为14,其离子方程式为Al+NO +OH-―→AlO
+OH-―→AlO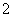 +NH3+N2+H2O(未配平)。还原产物是________。若除去0.2 mol NO
+NH3+N2+H2O(未配平)。还原产物是________。若除去0.2 mol NO ,要消耗铝________g。
,要消耗铝________g。
(4)工业废水中常含有不同类型的污染物,可采用不同的方法处理。下列处理措施和方法中正确的是________。
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 碱性的废水 | 用CO2中和 | 化学法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 废酸 | 加生石灰中和 | 化学法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)25 ℃、101 kPa时,1 g甲醇完全燃烧生成CO2和液态水,放出22.68 kJ热量,则该反应的热化学方程式为________________________________________。
(2)0.3 mol气态高能燃料乙硼烷(B2H6)在O2中燃烧,生成固态B2O3和液态水,放出649.5 kJ热量,则该反应的热化学方程式为______________
______________________________________________________________。
(3)肼(N2H4)是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量,则肼燃烧的热化学方程式为______________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金。该电池在充电过程中的总反应方程式是:Ni(OH)2+M===NiOOH+MH
已知:6NiOOH+NH3+H2O+OH-===6Ni(OH)2+NO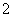
下列说法正确的是( )
A.NiMH电池放电过程中,正极的电极反应式为:NiOOH+H2O+e-===Ni(OH)2+OH-
B.充电过程中OH-离子从阳极向阴极迁移
C.充电过程中阴极的电极反应式:H2O+M+e-===MH+OH-,H2O中的H被M还原
D.NiMH电池中可以用KOH溶液、氨水等作为电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
回答下列问题:
(1)D2+的价层电子排布图为________。
(2)四种元素中第一电离能最小的是________,电负性 最大的是________。(填元素符号)
最大的是________。(填元素符号)
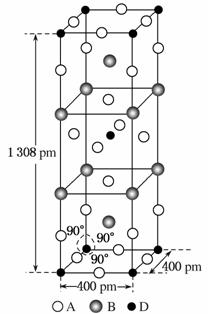
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
①该化合物的化学式为________;D的配位数为________;
②列式计算该晶体的密度________g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有________;该化合物中存在一个复杂离子,该离子的化学式为________,配位体是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂等的漂白与杀菌。下图是用过氧化氢法生产亚氯酸钠晶体的工艺流程图:
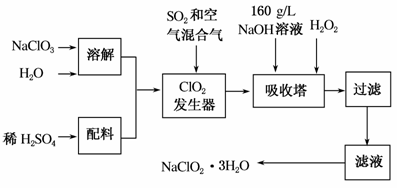
已知:①NaClO2的溶解度随温度升高而增大。
②纯ClO2气体易分解爆炸。
(1)发生器中鼓入空气的作用可能是________(填选项字母,下同)。
a.将SO2氧化成SO3,增强酸性
b.稀释ClO2以防止爆炸
c.将NaClO3氧化成ClO2
(2)吸收塔内发生反应的化学方程式为________________________ _________________。吸收塔内的温度不能超过20 ℃,原因是_____________________________________________________________。
(3)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是__________________________。
(4)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是________。
a.Na2O2 b.Na2S c.FeCl2
(5)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是________。
a.蒸馏 b.蒸发浓缩 c.灼烧 d.过滤
e.冷却结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液反应,产生CO2气体
B.乙酸酸性较弱,不能使紫色石蕊试液变红
C.乙酸分子中含有碳氧双键,所以它能与溴发生加成反应使溴水褪色
D.酯化反应不属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
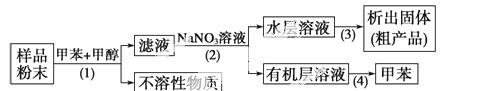
下列说法错误的是 ( )
A.步骤(1)需要过滤装置
B.步骤(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚
D.步骤(4)需要蒸馏装置
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com