
X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
A.XYZ2 B.X2YZ3
C.X2YZ2 D.XYZ3
科目:高中化学 来源: 题型:
写出具有下列分子式但仅有一个核磁共振信号的化合物的结构简式:
(1)C5H12:____________________________________________;
(2)C2H6O:___________________________________________;
(3)C2H4Br2:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展,像电一样,氢是一种需要依靠其他能源如石油、煤、原子能等的能量来制取的所谓“二次能源”,而存在于自然界的可以提供现成形式能量的能源称为一次能源,如煤、石油、太阳能和原子能等。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且原料可持续利用的制氢气的方法是( )
A.电解水 B.锌和稀硫酸反应
C.光解海水 D.以石油、天然气为原料
(2)氢气燃烧时耗氧量小,发热量大。已知下列热化学方程式:C(g)+O2(g)===CO2(g)
ΔH=-393.5 kJ·mol-1 H2(g)+ O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是____________________________________________________。
(3)氢能源有可能实现能源的贮存,也有可能实现经济、高效的输送。研究表明过渡金属型氢化物(又称间充氢化物),在这类氢化物中,氢原子填充在金属的晶格间隙之间,其组成不固定,通常是非化学计量的,如:LaH2.76、TiH1.73、CeH2.69、ZrH1.98、PrH2.65、TaH0.78。已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为10.64 g/cm3,相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
a g某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了a g,下列物质不能满足上述结果的是( )
A.CO B.H2
C.C6H12O6 D.C12H22O11
查看答案和解析>>
科目:高中化学 来源: 题型:
对于第三周期从左到右的主族元素,下列说法中不正确的是( )
A.原子半径逐渐减小
B.电子层数逐渐增多
C.最高正化合价逐渐增大
D.元素的电负性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期金属元素甲~戊在元素周期表中的相对位置如下表所示。下列判断正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
A.原子半径:丙<丁<戊
B.金属性:甲>丙
C.氢氧化物碱性:丙>丁>戊
D.最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
我国稀土资源丰富。下列有关稀土元素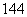 62Sm与
62Sm与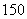 62Sm的说法正确的是( )
62Sm的说法正确的是( )
A.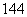 62Sm与
62Sm与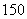 62Sm互为同位素
62Sm互为同位素
B.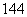 62Sm与
62Sm与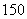 62Sm的质量数相同
62Sm的质量数相同
C.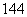 62Sm与
62Sm与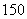 62Sm是同一种核素
62Sm是同一种核素
D.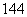 62Sm与
62Sm与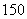 62Sm的核外电子数和中子数均为62
62Sm的核外电子数和中子数均为62
查看答案和解析>>
科目:高中化学 来源: 题型:
a、b、c、d、e、f、g为七种由短周期元素构成的微粒,它们都有10个电子,其结构特点如下:
| 微粒代码 | a | b | c | d | e | f | g |
| 原子核数目 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 带电荷数(单位电荷) | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
其中b的离子半径大于e的离子半径;d是溶于水显碱性的四原子分子;c与f作用可生成2个中性分子g。
试写出:
(1)a微粒的原子结构示意图为____________。
(2)b和e相应元素的最高价氧化物的水化物的碱性强弱比较为:________>________(用化学式表示)。
(3)d的水溶液显碱性的原因(用电离方程式表示)__________________。
(4)c微粒是________,f微粒是________(用化学式表示)。
(5)b相应的元素的单质与g微粒反应的化学方程式为
____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:

某课外活动小组用如图所示装置进行实验,请回答下列问题:
(1)若开始实验时开关K与a连接,则B极的电极反应式为________________________________________________________。
(2)若开始实验时开关K与b连接,则下列说法正确的是________(填序号)。
①溶液中Na+向A极移动
②从A极逸出的气体能使湿润的蓝色石蕊试纸先变红后褪色
③反应一段时间后向电解液中加适量盐酸可使其恢复到电解前的浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com