
ij�¶�ʱ����һ���ݻ�Ϊ2 L���ܱ������У�X��Y��Z���������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף�
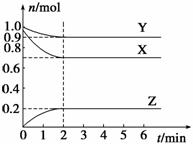
��1���÷�Ӧ�Ļ�ѧ����ʽΪ_______________��
��2����Ӧ��ʼ��2 min������Z�ķ�Ӧ����Ϊ____________��
��3����X��Y��Z��Ϊ���壬��Ӧ�ﵽƽ��ʱ��
��ѹǿ�ǿ�ʼʱ��________����
������ʱ�������������СΪԭ���� 0.5�����ﵽƽ��ʱ���������¶Ƚ�����(���������������Ƚ���)����÷�Ӧ������ӦΪ________��Ӧ(����ȡ������ȡ�)��
 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ʽ���һ��ȡ����Ӧ��ֻ���������ַе㲻ͬ���л�������ǣ� ��
A.��CH3��2CHCH2CH2CH3 B.��CH3��2CHCH3
C.��CH3��2CHCH��CH3��2 D.��CH3��3CCH2CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ���ѧ����������ᡢ�����������������ء������й�˵���д������
A��Һ�������������
B��С�մ���������θ�����
C����������������ˮ��ɱ������
D�������������Ʊ��轺��ľ�ķ������ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�Ȼ�ѧ����ʽ(Q1��Q2��Ϊ��ֵ)��
C(s)��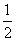 O2(g) ===CO(g) ��H����Q1 kJ��mol��1��C(s)��O2(g) ===CO2(g) ��H����Q2 kJ��mol��1��
O2(g) ===CO(g) ��H����Q1 kJ��mol��1��C(s)��O2(g) ===CO2(g) ��H����Q2 kJ��mol��1��
�й�������Ӧ�������������
A��Q1<Q2 B�������������������ڷ�Ӧ��������
C����1 mol C��Ӧ����1 mol CO����ʱ�ų�Q1 kJ������
D��1 mol CO2������е���������1 mol�ɱ����е�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪ij���淴Ӧ��mA(g)+nB(g)  pC(g) ��H=Q kJ��mol-1 �����ܱ������н��У���ͼ��ʾ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B�İٷֺ����Ĺ�ϵ���ߣ������ж���ȷ����
pC(g) ��H=Q kJ��mol-1 �����ܱ������н��У���ͼ��ʾ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B�İٷֺ����Ĺ�ϵ���ߣ������ж���ȷ����
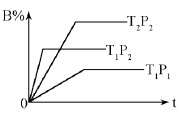
A��T2 >T1 P1 > P2 m+n > p �� ��<0
B��T1 >T2 P1 < P2 m+n < p �� ��>0
C��T1 <T2 P1 < P2 m+n < p �� ��<0
D��T1 >T2 P1 < P2 m+n > p �� ��>0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ����
A���Ҵ������Ͷ��ǿ�������Դ��Ӧ�����ƹ㡰�Ҵ����͡�
B����ӦNH3(g) + HCl (g)== NH4Cl(s)�������¿��Է����У���÷�Ӧ�ġ�H <0
C���õ��ˮ�ķ�����ȡ�����������Ի�����Դ���������
D�������¶Ȼ�ܽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ں����ܱ������з����Ŀ��淴ӦN2(g)��3H2(g)  2NH3(g)����H<0����˵����Ӧ�ﵽ��ѧƽ��״̬����(����)
2NH3(g)����H<0����˵����Ӧ�ﵽ��ѧƽ��״̬����(����)
A���Ͽ�1��N��N����ͬʱ��6��N��H������
B�����������ܶȲ���
C����������ƽ����Է�����������
D��N2��H2��NH3������֮��Ϊ1:3:2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ᣨHCN��������������,����֤������������ʵ���
A��HCN������ˮ
B��HCN��Һ�ܵ���
C��1mol/L��������Һ��pHԼΪ3
D��10 mL1 mol��L-1HCNǡ����10 mL 1 mol��L-1 NaOH��Һ��ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������Ƕ�Ӧ���ʵ��۵㣬�йص��жϴ�����ǣ����� ��
| Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
| 920�� | 97.8�� | 1291�� | 190�� | 2073�� | -107�� | -57�� | 1723�� |
�� A�����н��������ӵľ��岻һ�������Ӿ���
��B���ڹ��ۻ���������и�ԭ�Ӷ��γ�8���ӽṹ
��C��ͬ��Ԫ�ص���������γɲ�ͬ���͵ľ���
��D������������۵㲻һ���ȷ��Ӿ���ĸ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com