
°ŃŌŚæÕĘųÖŠ¾ĆÖƵÄĀĮʬ5£®0 gĶ¶ČėŹ¢ÓŠ500 mL 0£®5 mol ”¤L£1ĮņĖįČÜŅŗµÄÉÕ±ÖŠ£¬øĆĀĮʬÓėĮņĖį·“Ó¦²śÉśĒāĘųµÄĖŁĀŹvÓė·“Ó¦Ź±¼ätæÉÓĆČēĻĀ×ų±źĒśĻߥ“±ķŹ¾£ŗ
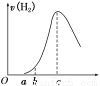
ĻĀĮŠĶĘĀŪ“ķĪóµÄŹĒ
A£®O”śa¶Ī²»²śÉśĒāĘųŹĒŅņĪŖ±ķĆęµÄŃõ»ÆĪļøōĄėĮĖĀĮŗĶĮņĖįČÜŅŗ
B£®b”śc¶Ī²śÉśĒāĘųµÄĖŁĀŹŌö¼Ó½ĻæģµÄÖ÷ŅŖŌŅņÖ®Ņ»ŹĒĪĀ¶ČÉżøß
C£®cµćŹ±·“Ó¦“¦Ę½ŗāדĢ¬
D£®t£¾c²śÉśĒāĘųµÄĖŁĀŹ½µµĶÖ÷ŅŖŹĒŅņĪŖČÜŅŗÖŠc£ØH£«£©½µµĶ
C
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗŌŚæÕĘųÖŠ¾ĆÖƵÄĀĮʬ±ķĆęÓŠŅ»²ćŃõ»ÆĤ¹Ź£®O”śa¶Ī²»²śÉśĒāĘųŹĒŅņĪŖ±ķĆęµÄŃõ»ÆĪļøōĄėĮĖĀĮŗĶĮņĖįČÜŅŗµÄ·“Ó¦£¬¹ŹAĻīĖµ·ØÕżČ·£»øĆ·“Ó¦·ÅČČ£¬Ėę×Å·“Ó¦½ųŠŠĪĀ¶ČÉżøߣ¬·“Ó¦ĖŁĀŹ¼Óæģ£¬¹ŹBĻīĖµ·ØÕżČ·£»Cµć·“Ó¦ĖŁĀŹ×īæģ£¬CµćŗóĖŁĀŹ¼õĀżŌŅņŹĒĖę×Å·“Ó¦½ųŠŠ·“Ó¦Īļc£ØH£«£©½µµĶĘšµ½Ö÷ŅŖ×÷ÓĆ£¬¹ŹDĻīĖµ·ØÕżČ·£»Cµć²¢²»ŹĒĘ½ŗāדĢ¬£¬¹ŹCĻīĖµ·Ø“ķĪ󣬱¾ĢāŃ”C”£
æ¼µć£ŗ»Æѧ·“Ó¦ĖŁĀŹĶ¼ĻńĪŹĢā”£


 ÓÅŅķŠ”°ļŹÖĶ¬²½æŚĖćĻµĮŠ“š°ø
ÓÅŅķŠ”°ļŹÖĶ¬²½æŚĖćĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŪ³ĮźĻŲµŚŅ»øßÖŠøßŅ»ÉĻµŚŅ»“Īæ¼ŹŌ»Æѧ£ØB£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¶ŌĪ£ĻÕ»ÆѧʷŅŖŌŚ°ü×°±źĒ©ÉĻÓ”ÓŠ¾ÆŹ¾ŠŌ±źÖ¾”£ĒāŃõ»ÆÄĘӦєÓƵıźÖ¾ŹĒ£Ø £©

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŹ”øßŅ»ÉĻµŚ¶ž“Īæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĄė×Ó·½³ĢŹ½ŹéŠ“ÕżČ·µÄŹĒ( )
A£®Ģ¼ĖįøĘÓėĻ”ŃĪĖį·“Ó¦£ŗCO32- + 2H+ = CO2”ü + H2O
B£®ĢśĘ¬ÓėĀČ»ÆĶČÜŅŗ·“Ó¦£ŗFe £«Cu2+ = Cu £«Fe2+
C£®ĒāŃõ»ÆĆ¾ČÜÓŚŃĪĖį£ŗMg£ØOH£©2£«2H+ = Mg2+ £«2H2O
D£®ĢśÓėĻ”ĮņĖį·“Ó¦£ŗ2Fe £«6H+ = 2Fe3+ £«3H2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŹ”øßŅ»ÉĻµŚ¶ž“Īæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¼ų±šĀČ»ÆĢśČÜŅŗÓėĒāŃõ»ÆĢś½ŗĢå×ī¼ņ±ćµÄ·½·ØŹĒ( )”£
A£®ŻĶČ” B£® ¹żĀĖ C£®ÕōĮó D£®¶”“ļ¶ūŠ§Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŹ”ø߶žÉĻѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠĶØČėX²¢·¢Éś·“Ó¦£ŗX(g)  2Y(g)£¬ĪĀ¶ČT1”¢T2ĻĀXµÄĪļÖŹµÄĮæÅضČc(X)Ėꏱ¼ät±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
2Y(g)£¬ĪĀ¶ČT1”¢T2ĻĀXµÄĪļÖŹµÄĮæÅضČc(X)Ėꏱ¼ät±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
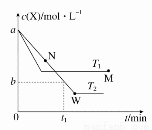
A£®øĆ·“Ó¦½ųŠŠµ½Mµć·Å³öµÄČČĮæŠ”ÓŚ½ųŠŠµ½Wµć·Å³öµÄČČĮæ
B£®T2ĻĀ£¬ŌŚ0”«t1Ź±¼äÄŚ£¬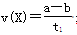 mol”¤L£1”¤min£1
mol”¤L£1”¤min£1
C£®MµćµÄÕż·“Ó¦ĖŁĀŹvÕżŠ”ÓŚNµćµÄÄę·“Ó¦ĖŁĀŹvÄę
D£®MµćŹ±ŌŁ¼ÓČėŅ»¶ØĮæX£¬Ę½ŗāŗóXµÄ×Ŗ»ÆĀŹ¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŹ”ø߶žÉĻѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀ±ķÖŠÓė»Æѧ·“Ó¦Ļą¶ŌÓ¦µÄ·½³ĢŹ½ÖŠ£¬ÕżČ·µÄŹĒ
Ń”Ļī | »Æѧ·“Ó¦ | Ąė×Ó·½³ĢŹ½ |
A | ŅŌŹÆÄ«×÷µē¼«µē½āĀČ»ÆÄĘČÜŅŗ | 2Cl- + 2H2O |
B | ŅŌŅų×÷µē¼«µē½āĻõĖįŅųČÜŅŗ | 4Ag++2H2O = 4Ag+O2”ü +4H+ |
C | Ē¦Šīµē³ŲÕż¼«·“Ó¦ | PbO2+4H++2e£ === Pb2++2H2O |
D | ĒāŃõČ¼ĮĻµē³Ų£ØKOH×öµē½āŅŗ£©øŗ¼«·“Ó¦ | O2 + 4e£+ 2H2O = 4OH£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŹ”øßŅ»ÉĻѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø15·Ö£©Š“³öĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½”£
£Ø1£©Na2CO3ČÜŅŗÓėŃĪĖįČÜŅŗ»ģŗĻ£ŗ £»
£Ø2£©ĮņĖįĶČÜŅŗŗĶĒāŃõ»Æ±µČÜŅŗ»ģŗĻ £»
£Ø3£©ĀČĘųÓėĒāŃõ»ÆÄĘČÜŅŗµÄ·“Ó¦ £»
£Ø4£©ĀČĘųÓėĖ®µÄ·“Ó¦ £»
£Ø5£©CO2ĘųĢåĶØČėµ½³ĪĒåŹÆ»ŅĖ®ÖŠ £»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŹ”øßŅ»ÉĻѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A£®1molOÖŹĮæŹĒ16g/mol
B£®22£®4L H2µÄĪļÖŹµÄĮæŹĒ1mol
C£®½«80gNaOHČÜÓŚ1LĖ®ÖŠ£¬ĖłµĆČÜŅŗÖŠNaOHµÄĪļÖŹµÄĮæÅØ¶ČŹĒ2mol/L
D£®NaClµÄĦ¶ūÖŹĮæŹĒ58£®5g/mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŹ”ĀåŃōŹŠøßŅ»10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ö»ÓĆĻĀĮŠŹŌ¼ĮÖŠµÄŅ»ÖÖ¾ĶÄܼų±šBa(NO3)2”¢Na2CO3”¢K2SO4ČżÖÖČÜŅŗ£¬ŌņøĆŹŌ¼ĮŹĒ( )
A£®KNO3ČÜŅŗ B£®Ļ”H2SO4
C£®NaOHČÜŅŗ D£®Na2SO4ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com