
| A. | 11.2 g | B. | 5.6g | C. | 8.4g | D. | 2.8g |
分析 所得溶液中加入KSCN溶液无血红色出现,则Fe、FeO、Fe2O3和Fe3O4组成的混合物与盐酸反应生成FeCl2,结合Fe原子守恒计算.
解答 解:Fe、FeO、Fe2O3和Fe3O4组成的混合物,加入100mL2mol/L的盐酸,混合物恰好完全溶解,所得溶液中加入KSCN溶液无血红色出现,混合物与盐酸反应生成FeCl2,若取等质量的该混合物,用足量的CO还原可得铁单质,由原子守恒可知Fe的物质的量等于的物质的量FeCl2,则存在2HCl~FeCl2~Fe,可知Fe的物质的量为0.1L×2mol/L×$\frac{1}{2}$=0.1mol,即取等质量的该混合物,用足量的CO还原可得铁单质的质量为0.1mol×56g/mol=5.6g,
故选B.
点评 本题考查化学反应方程式的计算,为高频考点,侧重于学生的分析与计算能力的考查,把握发生的反应、存在的关系式、原子守恒为解答该题的关键,题目难度不大.


 培优口算题卡系列答案
培优口算题卡系列答案科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素特征信息 |
| A | 最高正价和最低负价的绝对值之差为2 |
| B | 最外层电子数是内层电子数的3倍 |
| C | 1mol C单质能与冷水反应,在标准状况下生成11.2L H2 |
| D | 原子最外层电子数等于其周期序数 |
| E | 负二价阴离子的电子层结构与Ar原子相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第二周期第ⅡA族 | B. | 第三周期第ⅢA 族 | C. | 第三周期第ⅡA 族 | D. | 第二周期第ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨气能使湿润的蓝色石蕊试纸变红 | B. | 氨气极易溶于水,水溶液呈碱性 | ||
| C. | 氨和盐酸相遇能产生白烟 | D. | 氨水不稳定,受热易分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=CHCH3 | B. | CHCl=CHCl | C. | CH3CH=C(CH3)2 | D. | CH3CH2CH=CHBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
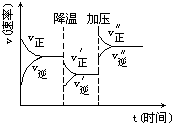 图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )| A. | A、B、C、D均为气体 | B. | 若A、B是气体,则C、D是液体或固体 | ||
| C. | 逆反应是放热反应 | D. | 在整个过程中,A的转化率一直增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:B>A,离子半径C<D | |
| B. | B的单质能与A的最高价氧化物发生置换反应 | |
| C. | 元素B和D能形成BD2型的共价化合物 | |
| D. | D的单质有毒,且干燥的单质D有漂白性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com