
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。其部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解产生大量白雾 ②易分解:SO2Cl2 |
回答下列问题:
I.已知:SO2(g)+Cl2(g) ![]() SO2Cl2(l) ΔH = 97.3 kJ·mol-1。催化合成硫酰氯的实验装置如下图 (夹持仪器已省略):
SO2Cl2(l) ΔH = 97.3 kJ·mol-1。催化合成硫酰氯的实验装置如下图 (夹持仪器已省略):

(1)仪器B的名称是____________,冷却水的进口为________(填“a”或“b”)。
(2)装置D除干燥气体外,另一作用是______________________。若缺少D,则硫酰氯会水解,该反应的化学方程式为_________________________________________。
(3)实验室用二氧化锰和浓盐酸反应制取氯气,写出其反应的离子方程式:__________________________________
(4)C处U形管中碱石灰的作用除吸收多余SO2、Cl2,防止污染外;还有_______________________。
II.在氯磺酸中加入四氯化锡加热煮沸,使氯磺酸分解,可用于制取少量硫酰氯。化学方程式为:2ClSO3H![]() H2SO4+SO2Cl2,此法得到的产品中混有硫酸。
H2SO4+SO2Cl2,此法得到的产品中混有硫酸。
(5)①从分解产物中分离出硫酰氯的方法是_____________。
②请设计实验方案检验产品中硫酸的存在(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):取适量产品,充分___________后,加水稀释__________________________。
【答案】冷凝管 a 通过观察气泡控制气流速度(或比例) SO2Cl2+2H2O==H2SO4+2HCl MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 防止水蒸气进入收集器使产品水解 蒸馏 加热 分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4
Mn2++Cl2↑+2H2O 防止水蒸气进入收集器使产品水解 蒸馏 加热 分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4
【解析】
由题意可知,甲装置中SO2与Cl2反应生成SO2Cl2,SO2、Cl2为有毒酸性气体,产物SO2Cl2易水解,所以仪器B中盛放的药品应为碱性物质碱石灰,其不仅可以防止空气中的水蒸气进入装置,还可以吸收SO2、Cl2,防止尾气污染。丁装置制取的Cl2中含有少量的HCl和水蒸气,装置丙的作用是除去HCl ,可使用饱和NaCl 溶液,装置乙的作用是除去水蒸气,可使用浓硫酸;若缺少装置乙,则硫酰氯会水解。为检验产品中有硫酸,可取产物在干燥条件下加热至完全反应(或挥发或分解等),冷却后加水稀释;取少量溶液滴加紫色石蕊试液变红;再取少量溶液,加入BaCl2溶液产生白色沉淀,说明含有H2SO4.
(1)根据装置图知仪器B的名称是冷凝管,冷却水的进口为a 进b 出。答案:冷凝管;a。
(2)装置D装的是浓硫酸,具有干燥气体的租用,还可以通过观察气泡控制气流速度(或比例)。若缺少D,硫酰氯会发生水解,该反应的化学方程式为SO2Cl2+2H2O==H2SO4+2HCl。答案:通过观察气泡控制气流速度(或比例);SO2Cl2+2H2O==H2SO4+2HCl。
(3)实验室用二氧化锰和浓盐酸反应制取氯气,其反应的离子方程式:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 。答案:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O 。答案:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
(4)C处U形管中碱石灰的作用除吸收多余SO2、Cl2,防止污染外;还可以防止水蒸气进入收集器使产品水解。
(5)①硫酸和硫酰氯沸点差别很大,故为了将硫酰氯和硫酸分离可采用蒸馏方法;答案:蒸馏。
②为检验产品中有硫酸,可取产物在干燥条件下加热至完全反应(或挥发或分解等),冷却后加水稀释;取少量溶液滴加紫色石蕊试液变红;再取少量溶液,加入BaCl2溶液产生白色沉淀,说明含有H2SO4。或取反应后的产物直接加BaCl2溶液,有白色沉淀,再滴加紫色石蕊试液变红,说明含有H2SO4。答案:分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4。


科目:高中化学 来源: 题型:
【题目】下列关于几种化学元素与植物代谢关系的叙述中,正确的是 ( )
A. O是组成糖类的基本元素之一,在有氧呼吸中CO2中的O来自丙酮酸
B. Fe是叶绿素的组成元素之一,没有Fe植物就不能进行光合作用
C. C是构成有机物的基本元素之一,可以在类囊体上通过光合作用形成有机物
D. P是构成ATP的必需元素之一,光合作用中只有光反应过程有ATP的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学—选修5:有机化学基础)
绿原酸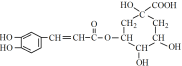 是一种抗氧化药物,存在下图转化关系。
是一种抗氧化药物,存在下图转化关系。
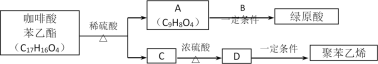
(1)绿原酸中的含氧官能团有:__________________________________。
(2)B的分子式是_____________________。
(3)C的氧化产物能发生银镜反应,则C的名称________________,写出C→D的化学方程式是______________________。
(4)咖啡酸苯乙酯的结构简式是___________________________________。
(5)F是A的同分异构体。F分别与碳酸氢钠溶液或新制Cu(OH)2反应产生气体或红色沉淀;苯环上只有两个取代基,且核磁共振氢谱表明该有机物中有8种不同化学环境的氢。
①符合上述条件的F有________种可能的结构。
②若F还能与NaOH在常温下以物质的量之比1∶2完全反应,其化学方程式是______(任写1个)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一恒容密闭容器中充入一定量的NO和炭粉,使之发生反应:C(s)+2NO(g)![]() CO2(g)+N2(g)ΔH,平衡时c(NO)与温度T的关系如图所示。下列说法正确的是
CO2(g)+N2(g)ΔH,平衡时c(NO)与温度T的关系如图所示。下列说法正确的是

A. ΔH>0
B. T2℃时,D点达到平衡时的平衡常数与B点的相等
C. 正反应速率:v(B)>v(D)>v(A)
D. 温度由T1升高到T3,NO的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 重水、超重水都是水的同位素
B. 正丁烷和异丁烷互为同分异构体
C. 金刚石、石墨和富勒烯均为碳的同素异形体,均属于原子晶体
D. 14C是指原子核内含有14个质子的碳的一种核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组溶液中的两个反应,可用同一离子方程式表示的是
A. CaCO3和HCl、Na2CO3和HCl B. BaCl2和H2SO4、Ba(OH)2和H2SO4
C. HNO3和K2CO3、HCl和NaHCO3 D. KOH和H2SO4、Ba(OH)2和HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碰撞理论是一种较直观的反应速率理论,下列有关碰撞理论叙述正确的是( )
A.分子发生碰撞就一定发生反应
B.发生有效碰撞的分子具有最高的能量
C.有效碰撞是活化分子在一定方向上的碰撞
D.活化分子的平均能量称之活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按要求书写
![]() 系统命名是________________________________
系统命名是________________________________
2—甲基—1,3-丁二烯的结构简式 __________________________________
(2)下列各对物质中属于同系物的是___________________,属于同分异构体的是____________属于同位素的是__________,属于同素异形体的是___________
A ![]() C与
C与![]() C B O2与O3
C B O2与O3
C  D
D 
E  与
与
(3)下列属于苯的同系物的是____________________(填字母)。
A  B
B ![]() C
C ![]() D
D 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.含有羟基的化合物一定属于醇类
B.代表醇类的官能团是与烃基或苯环侧链上的碳原子相连的羟基
C.酚类和醇类具有相同的官能团,因而具有相同的化学性质
D.分子内有苯环和羟基的化合物一定是酚类
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com