
| A. | 1 mol NO的质量是30g | |
| B. | 标准状况下,1 mol H2O的体积是22.4 L | |
| C. | 17 g NH3含有的氢原子总数为6.02×1023 | |
| D. | 0.1 mol Na2CO3中,Na+的物质的量为 0.1 mol |
分析 A.摩尔质量M=$\frac{m}{n}$,据此计算;
B.标准状况下水不是气体;
C.摩尔质量M=$\frac{m}{n}$=$\frac{N}{{N}_{A}}$,氨气分子中含3个氢原子;
D.离子物质的量=溶质物质的量×离子数.
解答 解:A.1 mol NO的质量=1mol×30g/mol=30g,故A正确;
B.标准状况下,1 mol H2O不是气体,所以其体积不是22.4 L,故B错误;
C.17 g NH3含有的氢原子总数=$\frac{17g}{17g/mol}$×3×6.02×1023=3×6.02×1023,故C错误;
D.0.1 mol Na2CO3中,Na+的物质的量为 0.2 mol,故D错误;
故选A.
点评 本题考查了物质的量的计算应用,物理量的计算等,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
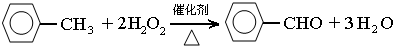
 苯甲醛(
苯甲醛(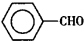 )、苯甲酸(
)、苯甲酸(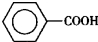 )都是重要的化工原料,都可用甲苯(
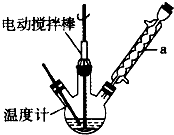
)都是重要的化工原料,都可用甲苯(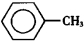 )为原料生产.下表列出了有关物质的部分物理性质,请回答:
)为原料生产.下表列出了有关物质的部分物理性质,请回答:| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度 ρ水=1g/cm3 | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
| 苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃,1.01×105Pa,64 g SO2中含有的原子数为3NA | |
| B. | 常温常压下,1.06 g Na2CO3含有的Na+个数为0.02NA | |
| C. | 常温常压下,32 g O2和O3的混合气体所含原子数为2NA | |
| D. | 含有NA个氧原子的氧气在标准状况下的体积为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
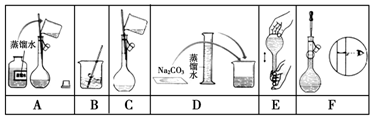
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 改变的条件 | 结论 |
| A | 升温 | CO32-的水解平衡向右移动 |
| B | 加入AlCl3固体 | 产生大量气体 |
| C | 加入100mLH2O | 溶液中c(H+)、c(OH-)均减小 |
| D | 加入少量CH3COONa固体 | 溶液中n(CO32-)增大 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com