
 ��
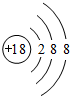
�� ���� A��B��C��D��E����Ԫ�ص�ԭ��������������Aԭ�������ӣ���AΪHԪ�أ�B�ĵ����ڿ����к�����࣬��BΪN��C��DԪ��ͬ������ԭ������DΪC�Ķ�������CΪOԪ�ء�DΪSԪ�أ�EԪ�ص���Χ�����Ų�Ϊ��n-l��dn+6nsl����n+6=10����n=4��������Χ�����Ų�Ϊ3d104sl����EΪCu���ݴ˽��н��
��� �⣺A��B��C��D��E����Ԫ�ص�ԭ��������������Aԭ�������ӣ���AΪHԪ�أ�B�ĵ����ڿ����к�����࣬��BΪN��CΪOԪ�ء�DΪSԪ�أ�EԪ�ص���Χ�����Ų�Ϊ��n-l��dn+6nsl����n+6=10����n=4��������Χ�����Ų�Ϊ3d104sl����EΪCu��
��1��BΪNԪ�أ��������ڱ��еڶ�����VA�壻
DΪS��ԭ�Ӻ��⺬��16�����ӣ���3���Ų������̬ԭ�ӵĵ����Ų�ʽΪ��1s22s22p63s23p4��
�ʴ�Ϊ���ڶ�����VA�壻1s22s22p63s23p4��
��2��EΪCuԪ�أ���4s���ȫ�գ�3dȫ�������Ϻ��ع��Ƚ��ȶ�������CuԪ�����γ�Cu+��
�ʴ�Ϊ��4s���ȫ�գ�3dȫ�������Ϻ��ع��Ƚ��ȶ���
��3��A��C�ֱ�ΪH��OԪ�أ�H��OԪ���ܹ��γɵĻ�������ˮ��˫��ˮ������ԭ�Ӹ�����Ϊ1��1�Ļ�����Ϊ˫��ˮ��˫��ˮΪ���ۻ���������ʽΪ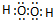 ��
��
�ʴ�Ϊ��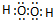 ��
��
���� ���⿼����λ�á��ṹ�����ʹ�ϵ��Ӧ�ã���Ŀ�Ѷ��еȣ��ƶ�Ԫ��Ϊ���ؼ���ע����������ԭ�ӽṹ��Ԫ�������ɡ�Ԫ�����ڱ��Ĺ�ϵ������������ѧ���ķ������������Ӧ��������


 ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | O |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� | �� | �� |
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
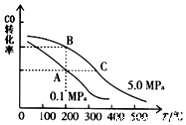 �о�����ȿ���CO��CO2��Ӧ�öԹ�����̬������������Ҫ�����壮
�о�����ȿ���CO��CO2��Ӧ�öԹ�����̬������������Ҫ�����壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
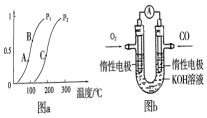 ������ʹ�������Դ��չ����̼���á�������Ϊ��ѧ���о�����Ҫ���⣮�������״������ʵ����ȼ�ϣ�������ȼ�ϵ�أ�
������ʹ�������Դ��չ����̼���á�������Ϊ��ѧ���о�����Ҫ���⣮�������״������ʵ����ȼ�ϣ�������ȼ�ϵ�أ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
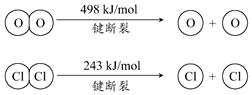 ��Cl2����ijЩ�����л���ʱ�����������HCl���������·�Ӧ����ʵ���ȵ�ѭ�����ã�
��Cl2����ijЩ�����л���ʱ�����������HCl���������·�Ӧ����ʵ���ȵ�ѭ�����ã�| A�� | �����¶������HCl��ת���� | |
| B�� | �����������ʹ�÷��˵��ʱ��С | |
| C�� | 1molCl2ת��Ϊ2molClԭ�ӷų�243kJ���� | |
| D�� | ����H2O��g����1mol H-O���ȶ���HCl��g����1mol H-Cl������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ������Һ | B�� | ����� | C�� | ����������Һ | D�� | �Ȼ�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͨ���� | B�� | ���� | C�� | Ư�� | D�� | �ɱ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
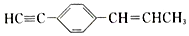 ��˵���в���ȷ���ǣ�������
��˵���в���ȷ���ǣ�������| A�� | ���ֻ��5��̼ԭ����ͬһֱ���� | B�� | �����11��̼ԭ����ͬһƽ���� | ||
| C�� | ��7��̼ԭ�ӿ�����ͬһֱ���� | D�� | �����19��ԭ����ͬһƽ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com