
 ��ͼ��ʾװ�ã��ش��������⣺
��ͼ��ʾװ�ã��ش��������⣺���� ��1��ͨ����е�⣬���ֱ���f���ȱ��ɫ����f�缫���������ӵõ��ӵĻ�ԭ��Ӧ���õ缫������������N�Ǹ�����M��������a��������b��������c��������d��������e�����������ݵ缫��Ӧʽ��ϵ����غ�֪ʶ�����㣻
��2�������϶�ͭ�����������������ͭ�Ǹ�����������Ǻ���ͭ���ӵĿ����Ե��Σ����ݵ�ƳصĹ���ԭ�����ش�
��3���ڵ��ص������ϵĽ������������÷���������Ϊ�����籣������
��� �⣺ͨ����е�⣬���ֱ���f���ȱ��ɫ����f�缫���������ӵõ��ӵĻ�ԭ��Ӧ���õ缫������������N�Ǹ�����M��������a��������b��������c��������d��������e��������
��1����ֱ����Դ��M�����������ʴ�Ϊ������
�ڼ׳�a�缫���������������ӵķŵ�˳�缫�ϵĵ缫��ӦʽΪ��4OH--4e-=2H2O+O2�����ʴ�Ϊ��4OH--4e-=2H2O+O2����
�۶��Ե缫�������������Һ��ʵ���ǵ��ˮ�����Ե���pH���ʴ�Ϊ�����׳ص��ˮ��c��NaOH������pH����
�����������ͨ��4mol���ӣ���װ�õ���ʵ���ǵ��ˮ�����Ա�����Һ������С��ת�Ƶ���4mol������ˮ2mol��������36g���ʴ�Ϊ����С��36g��
��2�������϶�ͭ�������������������f�缫��e�缫������Ϊͭ��������Ǻ���ͭ���ӵĿ����Ե���ͭ�����Һ��ͭ����Ũ�ȱ��ֲ��䣬�ʴ�Ϊ��ͭ��CuSO4��������ͭ�������䣻
��3���ñ�װ�ö����ĸ�ʴ���з������������Ӧ������������fΪ���缫���ñ���������Ϊ����ӵ��������������ʴ�Ϊ��f����ӵ�������������
���� ����Ϊ�绯ѧ֪ʶ���ۺ�Ӧ�ã�����ʱҪע����ݵ缫��Ӧ�����жϳ����ص��������������жϳ���Դ����������Ҫע����������Ϊ������·�����缫�ϵ�ʧ���ӵ���Ŀ��ȣ�����ʱҪ��ȷд���缫����ʽ��ȷ�ж����������ӵķŵ�˳��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Y����ͻ��ϼ�Ϊ-2����Z����������ϼ�Ϊ+6 | |
| B�� | ��X����������ϼ�Ϊ+5��������Ԫ�ض��Ƿǽ���Ԫ�� | |
| C�� | ��R��OH��n Ϊǿ���W��OH��n+1ҲΪǿ�� | |
| D�� | ��HnXOmΪǿ�ᣬ��Y�ǻ��÷ǽ���Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ӧ | B�� | ��ԭ��Ӧ | C�� | ��ȥ��Ӧ | D�� | ������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
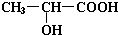 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij��ѧС��ͨ���������ϣ����������ͼ��ʾ�ķ����Ժ����ϴ���Ϊԭ�����Ʊ�NiSO4•7H2O����֪ij�������ĺ����ϴ�����Ҫ����Ni��������Al��31%����Fe��1.3%���ĵ��ʼ�����������������ʣ�3.3%����
ij��ѧС��ͨ���������ϣ����������ͼ��ʾ�ķ����Ժ����ϴ���Ϊԭ�����Ʊ�NiSO4•7H2O����֪ij�������ĺ����ϴ�����Ҫ����Ni��������Al��31%����Fe��1.3%���ĵ��ʼ�����������������ʣ�3.3%����| ������ | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
| Al��OH��3 | 3.8 | 5.2 |
| Fe��OH��3 | 2.7 | 3.2 |
| Fe��OH��2 | 7.6 | 9.7 |
| Ni��OH��2 | 7.1 | 9.2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com