
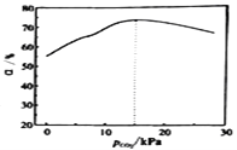
【题目】某兴趣小组用数字实验系统测定一定浓度碳酸钠溶液的pH与温度的关系,得到如图所示曲线。下列分析不正确的是
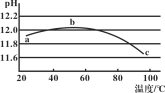
A.b点溶液中OH-浓度在整个过程中最大
B.水的电离平衡也会对溶液的pH产生影响
C.a→b段水解平衡向右移动
D.a点溶液显碱性,且离子浓度从大到小为:Na+>CO32->OH->HCO3-
【答案】A
【解析】
溶液中存在碳酸根的水解平衡CO32-+H2OHCO3-+OH-和水的电离平衡H2OH++OH-,图中显示温度升高溶液的碱性先增强后减弱,水的电离是吸热过程,纯水中温度升高pH值会降低,碳酸钠溶液中温度升高pH有增大的过程,说明水解受到促进,即水解为吸热过程;后pH值下降,说明温度升高水电离出更多的氢氧根抑制了碳酸根的水解,据此分析解答。
A. 温度升高,碳酸钠溶液中CO32-的水解程度增大,溶液中的OH-浓度会变大,则b点溶液中OH-浓度在整个过程中不是最大,故A错误;
B. 随温度升高,此时促进盐类水解,对水的电离也起到促进作用,水电离出的氢氧根离子浓度抑制了碳酸盐的水解平衡,导致溶液pH值减小,因此水的电离平衡也对pH产生影响,故B正确;
C. 水解是吸热过程,温度越高,水解程度越大,故a→b段水解平衡向右移动,故C正确;
D. 整个过程中溶液均呈碱性,故a点溶液显碱性,溶液中存在![]() 、
、![]() 、
、![]() ,且电离和水解程度较小,则离子浓度从大到小为:Na+>CO32->OH->HCO3-,故D正确;
,且电离和水解程度较小,则离子浓度从大到小为:Na+>CO32->OH->HCO3-,故D正确;
故选A。


科目:高中化学 来源: 题型:
【题目】(1)按要求完成下列问题:
① 甲基的电子式_________;
② 写出制备TNT的化学方程式__________;
③ 写出实验室制乙炔的化学方程式__________;
④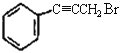 含有的官能团的名称为__________;
含有的官能团的名称为__________;
(2)某有机物的结构简式为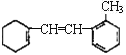 ,据此填写下列空格。
,据此填写下列空格。
① 该物质苯环上一氯代物有__________种;
② lmol该物质和溴水混合,消耗Br2的物质的量为__________mol;
③ lmol该物质和H2加成需H2__________mol。
(3)![]() 与一定量的Br2发生加成反应,生成的产物可能是_______。
与一定量的Br2发生加成反应,生成的产物可能是_______。
A.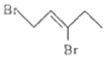 B.
B.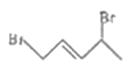
C.![]() D.
D.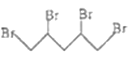
(4)实验证实,烯烃被酸性高锰酸钾溶液氧化时有如下规律:

己知某烃在通常情况下,只能跟等物质的量的溴反应:它与酸性高锰酸钾溶液反应时,所得氧化产物只有一种且没有支链,又知该烃充全燃烧时所需氧气的体积是相同状况下烃蒸气的8.5倍,试分析该烃的结构简式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.可以用丁达尔效应区分氯化铝溶液和氯化钠溶液
B.二氧化硅是一种酸性氧化物,故不能和酸发生反应
C.NaCl饱和溶液中依次通入足量的NH3、CO2,可析出NaHCO3
D.可以通过电解熔融氯化铝的方法来制备铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一“铁链”图案,图案上由左到右分别写了H2O、CO2、Na2O、NaCl、FeCl35种物质,图中相连的两种物质均可归属为一类,相交部分由左到右A、B、C、D为其相应的分类依据代号。请回答下列问题:

(1)请将分类依据代号填入相应的括号内:
(____)两种物质都是非金属氧化物
(____)两种物质都是钠的化合物
(____)两种物质中一种是酸性氧化物,一种是碱性氧化物
(____)两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入图中某种物质M的水溶液,继续煮沸可制得一种红褐色胶体。
①物质M的化学式为________。
②证明有红褐色胶体生成的最常用的实验操作是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据下图所示实验装置,回答下列问题。
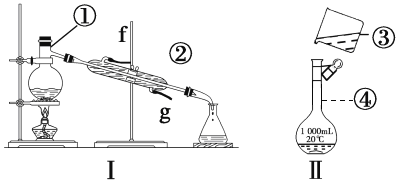
(1)写出下列仪器的名称:
①_____________②________________,④______________________
(2)仪器①~④中,使用时必须检查是否漏水的是_______________________(填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器________________,将仪器补充完整后进行的实验操作的名称为__________________②的进水口是____________(填“f”或“g”)。
(4)现需配制250mL、0.2mol·L1NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误操作:_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯是一种重要的化工原料,可采用乙苯催化脱氢法制备,反应如下:![]() (g)
(g)![]()
![]() (g)+H2(g) ΔH = +117.6kJ·mol-1
(g)+H2(g) ΔH = +117.6kJ·mol-1
(1)往刚性恒容容器中同时通入乙苯和水蒸气,测得容器总压和乙苯转化率随时间变化结果如图所示。
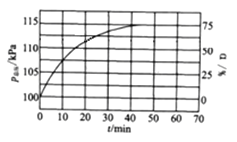
①平衡时,p(H2O)=_________,平衡常数Kp=_________kPa(Kp为以分压表示的平衡常数,请列式计算)
②下列说法正确的是_________
A.当混合气体的平均相对分子质量不再改变,反应达到平衡状态
B.增加通入水蒸气的量,有利于乙苯转化率的高
C.若将该反应置于恒压容器中反应,其他起始条件相同,乙苯的转化率将减小
D.仅往该刚性恒容容器中通入和上述等量的乙苯,其他条件相同,平衡时氢气的分压不变
(2)CO2气氛下乙苯催化脱氢可同时存在以下两种途径:

①请画出途径1的能量和反应过程的图像,并作适当标注______________

②途径I的反应历程如图所示,下列说法正确的是_________

A. CO2为氧化剂
B. 状态1到状态2形成了O-H键
C. 中间产物只有(![]() )
)
D. 该催化剂可提高乙苯的平衡转化率
③刚性容器中,在催化剂作用下,一定时间内p(CO2)与乙苯转化率关系如图分析,则p(CO2)为15kPa时,乙苯转化率最高的可能原因_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA为阿伏伽德罗常数的值。下列说法不正确的是( )
A. 12g金刚石中平均含有2NA个σ键
B. 1mol SiO2晶体中平均含有4NA个σ键
C. 12g石墨中平均含1.5NA个σ键
D. 1mol CH4中含4NA个s﹣p σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将13.0 g锌投入250mL某浓度的盐酸中,锌和盐酸恰好完全反应。求:
(1)反应中生成的H2在标准状况下的体积。__
(2)所用盐酸中HCl的物质的量浓度。_____________
(3)需用多少体积的36.5%的浓盐酸(ρ =1.20 g/mL)来配置上述盐酸。_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com