
(15分)化合物F是合成抗过敏药孟鲁司特钠的重要中间体,其合成过程如下:
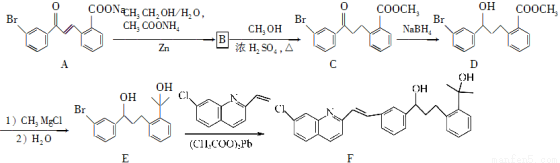
请回答下列问题:
(1)化合物C中含氧官能团为________、________(填名称)。
(2)化合物B的分子式为C16H13O3Br,则B的结构简式为____________。
(3)由C→D、E→F的反应类型依次为________、________。
(4)写出符合下列条件C的一种同分异构体的结构简式:______________。
Ⅰ.属于芳香族化合物,且分子中含有2个苯环;
Ⅱ.能够发生银镜反应;
Ⅲ.分子中有5种不同环境的氢原子。
(5)已知:RCl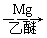 RMgCl,写出以CH3CH2OH、
RMgCl,写出以CH3CH2OH、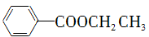 为原料制备
为原料制备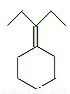 的合成路线流程图(乙醚溶剂及无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(乙醚溶剂及无机试剂任用)。合成路线流程图示例如下:
H2C=CH2 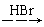 CH3CH2Br
CH3CH2Br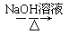 CH3CH2OH
CH3CH2OH
科目:高中化学 来源:2014-2015学年山东齐鲁名校教科研协作体19所名校高三第二次调研化学试卷(解析版) 题型:选择题
在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应X(g)+Y(g) 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:

下列说法不正确的是
A.反应前2 min的平均速率υ(Z)=2.0×10—3mol/(L·min)
B.其他条件不变,升高温度,反应达到新平衡前υ(逆)>υ(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省“江淮十校”高三4月联考理综化学试卷(解析版) 题型:简答题
湿式吸收一电解再生法,是采用氧化一电解的双反应器对含硫化氢的废气进行脱硫制氢。实验表明,双反应器法可以在较宽的范围内实现对硫化氢的有效吸收,并可同时制取氢气和硫磺,该法基本流程见图l,其中氧化吸收器中为FeCl3溶液,电解反应器可实现FeCl3溶液的恢复及H2的制备。
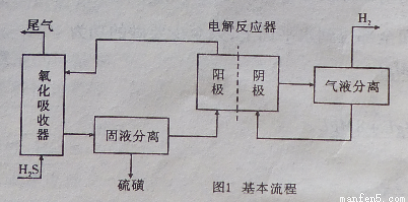
(1)氧化反应器中发生的主要反应的离子有程式为________
(2)电解反应器中,阳极反应式是________
(3)某研究小组在实验室中模拟上述过程,研究FeCl3溶液吸收H2S气体的效率,实验时要先向FeCl3溶液中通人N2,其目的是 ________ 。对影响吸收效率的因素提出如下假设,请你完成假设二和假设三:
假设一:H2S气体的通入速率;
假设二: ;
假设三: .
请你设计实验就假设一进行验证,将实验步骤及结论补充完整(注:可用pH计测量溶液中的H+浓度)

(4)将FeCl3溶液吸收H2S气体后的溶液过滤后,取少量向其中加入BaCl2溶液,发现有白色沉淀生成(注:BaS溶于盐酸)。则白色沉淀可能是_______你的判断理由是_______
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市、石嘴山市高三四月联考理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.常温下,在0.1mol·L-1的HNO3溶液中,由水电离出的c(H+)<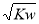
B.浓度为0.1mol·L-1的NaHCO3溶液:c(H2CO3)>c(CO32-)
C.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
D.冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省泰州市高三第二次模拟考试化学试卷(解析版) 题型:实验题
【实验化学】硫酸锌是一种重要的工业原料。在实验室从粗锌(含有少量的铅)与稀硫酸反应后的废液中提取硫酸锌的主要操作步骤如下:
步骤1:将废液过滤,调节滤液的pH约为2,过滤,将滤液加热浓缩,制得较高温度下的饱和溶液,冷却结晶得到粗制晶体。
步骤2:①在烧杯中用蒸馏水溶解步骤1得到的晶体,滴加少量稀硫酸,水浴加热至晶体全部溶解。
②停止加热,让其自然冷却、结晶。
③抽滤,用少量无水乙醇洗涤晶体1~2次,得精制晶体。
(1)废液中含有的不溶性杂质是________。
(2)步骤1中调节滤液pH约为2,可加入的物质是________(填字母)。
a.NH3·H2O b.ZnO c.ZnCO3 d.NaOH
(3)步骤1中对滤液加热浓缩时,当________时,停止加热。
(4)步骤2中滴加少量稀硫酸的目的是____。
(5)抽滤装置如图所示,仪器B的名称是________。仪器C的作用是____________。
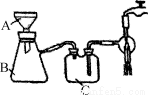
(6)用少量无水乙醇洗涤晶体的目的是________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省泰州市高三第二次模拟考试化学试卷(解析版) 题型:选择题
下列有关实验操作对应的现象及对现象的解释或所得出的结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 向浓度均为0.1 mol·L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
B | 溴乙烷与NaOH溶液共热后,滴加AgNO3溶液 | 未出现淡黄色沉淀 | 溴乙烷未水解 |
C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中不含K+ |
D | 某盐溶于盐酸,产生无色无味气体通入澄清石灰水 | 变浑浊 | 说明该盐是碳酸盐 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省泰州市高三第二次模拟考试化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值。下列说法正确的是
A.1 mol Cl2与足量的Fe充分反应,转移电子的数目为3NA
B.常温下,1 L pH=1的H2SO4溶液中,由水电离出的H+数目为0.1NA
C.常温下,21 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D.1 mol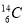 原子中所含中子数目为6NA
原子中所含中子数目为6NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南通、扬州、连云港高三第二次调研测试化学试卷(解析版) 题型:选择题
已知X、Y、Z、W、R是原子序数依次增大的五种短周期主族元素,其中Y、R原子最外层电子数相等;X元素最低负价与W元素最高正价绝对值相等;工业上常用电解熔融氧化物的方法冶炼W单质;Z、W、R最高价氧化物对应的水化物两两反应均生成盐和水。下列说法正确的是
A.简单离子半径:Y>Z>W
B.简单氢化物的热稳定性:X>Y>R
C.W的最高价氧化物对应的水化物碱性比Z的强
D.R的最高价氧化物对应的水化物化学式一定是HRO4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三第二次模拟考试理综化学试卷(解析版) 题型:实验题
(16分)某校研究性学习小组在实验室中模拟侯氏制碱法制取少量纯碱(见下图),并测定纯碱的纯度。回答下列问题:
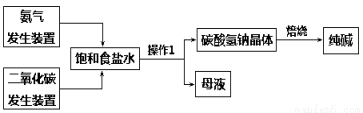
Ⅰ.纯碱的制备
(1)若上述两个气体发生装置相同,制取二氧化碳的试剂为大理石和稀盐酸,制取氨气宜选择的试剂为 。氨气和二氧化碳在通入饱和食盐水时的顺序是(填序号) 。
a.同时通入
b.先通氨气至饱和再通二氧化碳
c.先通二氧化碳至饱和再通氨气
(2)他们采用粗盐配制饱和食盐水。粗盐中含有Ca2+、Mg2+、SO42—等杂质离子,除去这些杂质离子需要下列试剂:①Na2CO3溶液 ②NaOH溶液 ③BaCl2溶液 ④盐酸。加入这些试剂的顺序可以是(填序号) 。
a. ①③②④ b. ③①④② c. ②③①④ d. ③②①④
(3)操作1的名称叫 。为洗去碳酸氢钠晶体表面的残留母液,他们用酒精代替水洗,其优点是 。
Ⅱ.纯碱纯度的测定(注:只考虑其中因焙烧不充分而含有的碳酸氢钠,忽略其他杂质)
(1)该小组同学设计了如下方案,其中不可行的是(填序号) 。
A、准确称量mg样品,加热至恒重,称量得ng固体。
B、准确称量mg样品,与足量稀硫酸反应,将产生的气体用碱石灰吸收,碱石灰增重ng。
C、准确称量mg样品,与足量氢氧化钡溶液反应,过滤、洗涤、干燥,称量得ng固体。
(2)若方案A可行,加热过程中所需仪器除了酒精灯、三角架、坩埚、坩埚钳外,还需 。
(3)若方案B正确,涉及反应的离子方程式为 。
(4)若方案C可行,判断沉淀是否洗净的方法是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com