
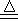 ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(
ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(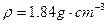 )110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
)110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题



| 物质 | 蛋白质溶液 (氯化钠溶液) | 乙 烷 (乙烯) | 肥 皂 (甘油) | 乙醇(水) | 乙酸乙酯(乙酸) | 溴苯(溴) |
| 加入试剂 | | | | | | |
| 操作方法 | | | | | | |
查看答案和解析>>
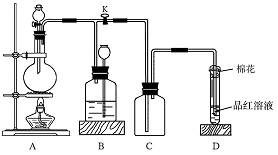
科目:高中化学 来源:不详 题型:实验题
 仪器如图所示(装置可重复使用)。回答下列问题:
仪器如图所示(装置可重复使用)。回答下列问题: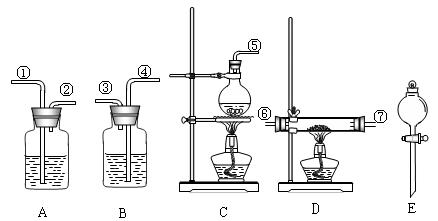
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ |
| B.②③④ |
| C.①③④ |
| D.④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.没有难溶、难电离、易挥发物质生成的复分解反应也可能发生 |
| B.溶液中某些离子结合成新物质析出,其根本原因是这些离子浓度的幂次积超过了该物质的溶度积常数或电离平衡常数 |
| C.一种难溶物质或难电离物质,可以通过复分解反应生成更难溶或更难电离的物质 |
| D.只要适当改变温度、压强、浓度,任何反应都可自发进行 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
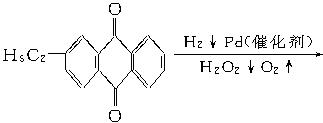
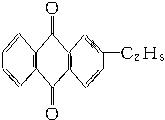

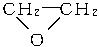 +CaCl2+H2O,则制备
+CaCl2+H2O,则制备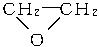 工艺的原子利用率为
工艺的原子利用率为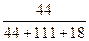 ×100%。在绿色化学工艺中,原子的利用率为100%的工艺称理想状态的“绿色工艺”。本题提供的生成H2O2的方法,可否称为理想状态的“绿色工艺”?简述理由。
×100%。在绿色化学工艺中,原子的利用率为100%的工艺称理想状态的“绿色工艺”。本题提供的生成H2O2的方法,可否称为理想状态的“绿色工艺”?简述理由。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.以焦炭和水制取水煤气后分离出氢气 |
| B.用铁、锌等活泼金属与稀硫酸反应制取氢气 |
| C.由火力发电厂提供电力电解水产生氢气 |
| D.利用高效催化剂和太阳能使海水分解产生氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com