
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲?乙?丙?戊是由其中的两种或三种元素组成的化合物,丁是由Z元素形成的单质。已知:甲+丙→丁+己,甲+乙→戊+丁;25℃时0.01mol·L-1己溶液的pH为12。下列说法不正确的是( )
A.1.0L 0.1mol·L-1戊溶液中阴离子总的物质的量大于0.1mol
B.将足量甲加入到酚酞试液中,溶液先变红后褪色
C.X与W构成的化合物、戊、己均为离子化合物
D.W的简单离子半径大于Z的简单离子半径
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源:2015-2016学年湖北沙市高二下第四次半月考化学试卷(解析版) 题型:推断题
下表是A、B、C、D、E五种有机物的有关信息:
A | B | C | D | E |
①能使溴的四氯化碳溶液褪色 ②比例模型为:
③能与水在一定条件下反应生成C | ①由C、H两种元素组成 ②球棍模型为:
| ①能与钠反应,但不能与NaOH溶液反应; ②能与E反应生成相对分子质量为100的酯 | ①由C、H、Br三种元素组成; ②相对分子质量为109 | ①由C、H、O三种元素组成; ②球棍模型为:
|
根据表中信息回答下列问题:
(1)写出A使溴的四氯化碳溶液褪色的化学方程式:________________________;
(2)A与氢气发生加成反应后生成分子F,F的同系物的通式为CnH2n+2。当n =________时,这类有机物开始有同分异构体。
(3)B的分子式为________,写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:___ ;
(4)D→A所加试剂及反应条件为____________________;反应类型为__________________;
(5)C与E反应能生成相对分子质量为100的酯,写出该反应的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北沙市高二下第四次半月考化学试卷(解析版) 题型:选择题
下面的排序正确的是( )
A.硬度由大到小:金刚石>碳化硅>晶体硅 B.熔点由高到低:SiC>Si>SiO2>Ge
C.沸点由高到低:NH3>PH3>AsH3>SbH3 D.晶格能由大到小:NaI>NaBr>NaCl>NaF
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三5月月考理综化学试卷(解析版) 题型:填空题
雾霾天气肆虐给人类健康带来了严重影响。燃煤和汽车尾气 是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g) 2C02(g)+N2 (g) △H <0 。
2C02(g)+N2 (g) △H <0 。
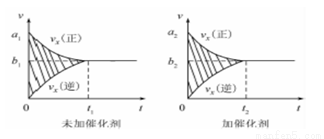
①该反应的速率时间图像如右图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,则其速率时间图像如右图中右图所示。以下说法正确的是 (填对应字母)。
A.a1>a2 B.b1 <b2 C.t1>t2
D.右图中阴影部分面积更大 E.左图中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。

(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。已知:CH4(g)+2N02(g) = N2(g)+C02(g)+2H20(g) △H=-867 kJ/mol
2N02(g)= N204(g) △H= - 56.9 kJ/mol H20(g) = H20(l) △H = - 44.0 kJ/mol
写出CH4催化还原N204 (g)生成N2和H20(1)的热化学方程式: 。
(3)CH4和H20(g)在催化剂表面发生反应CH4 + H20 = C0 + 3H2 ,该反应在不同温度下的化学平衡常数如下表:
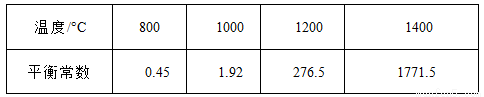
①该反应是 反应(填“吸热”或“放热 ”)。
②T℃时,向1L密闭容器中投入1mol CH4 和1mol H20(g),平衡时C(CH4)=0.5 mol·L-1 , 该温度下反应CH4 + H20 = CO+3H2的平衡常数K= 。
(4)甲烷燃料电池可以提升能量利用率。如图是利用甲烷燃料电池电解100mL lmol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24 L(设电解后溶液体积不变)。

①甲烷燃料电池的负极反应式: 。
②电解后溶液的pH = , (忽略氯气与氢氧化钠溶液反应)。
③阳极产生气体的体积在标准状况下是 L。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:实验题
【化学–选修5:有机化学基础】
有机物G是某种新型药物的中间体,其合成路线如下:
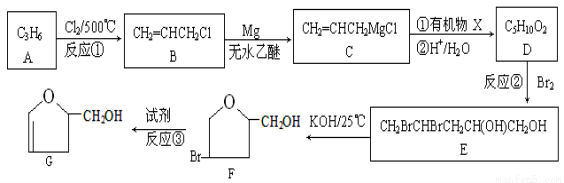
已知: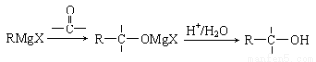
回答下列问题:
(1)写出反应③所需要的试剂 ;反应①的反应类型是 。
(2)有机物B中所含官能团的名称是 ;
(3)写出有机物X的结构简式 ;
(4)写出由E到F的化学方程式 ;
(5)写出所有同时符合下列条件的D的同分异构体的结构简式 ;
①能发生银镜反应; ②能发生水解反应
(6)以1-丙醇为原料可合成丙三醇,请设计合成路线(无机试剂及溶剂任选)。
已知:烯烃上的烷烃基在500℃与氯气发生取代反应。
注:合成路线的书写格式参照如下示例流程图:
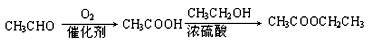
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是

A.镍是阳极,电极反应为4OH--4e一= O2↑+ 2 H2O
B.电解时电流的方向为:负极→Ni电极→溶液→Fe电极→正极
C.若隔膜为阴离子交换膜,则OH-自右向左移动
D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都七中高一下课后作业乙烯化学试卷(解析版) 题型:实验题
1,2-二溴乙烷在常温下是无色液体,密度是2.18g/cm3,沸点是131.4℃,熔点是9.79℃,不溶于水,易溶于醇、丙酮等有机溶剂.在实验室可用如图所示装置来制备1,2-二溴乙烷.其中试管c中装有浓溴水.
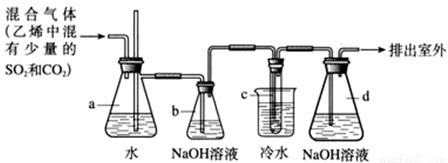
(1)写出制备1,2-二溴乙烷的化学方程式:_____________________。
(2)安全瓶a可以防止倒吸,并可以检查实验进行时试管c是否发生堵塞。如果发生堵塞,a中的现象是:______.
(3)容器b中NaOH溶液的作用是______,相应的离子方程式为________________,可能发生反应的离子方程式为__________________________。
(4)将试管c置于冷水中,以及液溴表面覆盖少量水的原因是:____________。
(5)某同学在做实验时,使用一定量的液溴,当溴全部褪色时,通入的乙烯混合气体的量比正常情况下超出许多。如果装置的气密性没有问题,试分析可能的原因:__________。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省师大一附高三5月月考理综化学试卷(解析版) 题型:填空题
自来水生产的流程示意图见下:
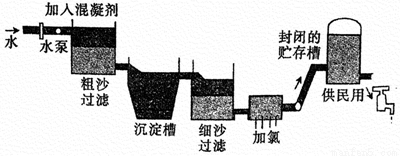
(1)二氧化氯(ClO2)是一种高效、安全的水处理剂,比C12好。有如下两种制备C1O2方法:
方法一:2NaClO3+4HCl=2C1O2↑+Cl2↑+2NaCl+2H2O
方法二:2NaC lO3 +H2O2+H2SO4=2C lO2↑ +Na2SO4十O2↑+2H2O
用方法二制备的C1O2更适合用于饮用水消毒,其主要原因是__________。
C1O2和C12在消毒时自身均被还原为Cl-, C1O2的消毒能力是等质量Cl2的_________倍
(2)含有较多的钙、镁离子的水被称为硬水。暂时硬水最常见的软化方法是_________。
永久硬水一般可以使用离子交换树脂软化,先把水通过装有_________ (填“阴”或“阳”)离子交换树脂的交换柱,再通过另一种功能的离子交换树脂。使用后的阳离子交换树脂可以置于_________中再生。
(3)水处理中常见的混凝剂有硫酸铝、聚合氛化铝、硫酸亚铁、硫酸铁等。硫酸亚铁作为混凝剂在除去悬浮物质时,需要将水的pH调至9左右,原因是_________。
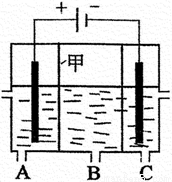
(4)电渗析法是一种利用离子交换膜进行海水淡化的方法.下图是电渗析法的示意图,淡水从_________(填“A”、“B”或,“C”)口流出,甲为_________离子交换膜。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com