
| 资料卡片 | ||
| 物质 | 熔点 | 沸点 |
| SiCl4 | -70℃ | 57.6℃ |
| TiCl4 | -25℃ | 136.5℃ |

| 11g |
| 44g/mol |
| ||
| ||
| 22.4L |
| 22.4L/mol |
| 11g |
| 44g/mol |
| 0.25mol |
| 1mol |


 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
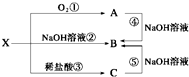 (1)写出下列物质的化学式:A:
(1)写出下列物质的化学式:A:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 生成的盐 | 化学式 | 质量/g |
| A | ||
| B |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H++OH-═H2O |
| B、CO32-+2H+═H2O+CO2↑ |
| C、Zn(OH)2+2H+═Zn2++2H2O |
| D、Cu2++2OH-+Ba2++SO42-═BaSO4↓+Cu(OH)2↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com