
| A. | 升高 | B. | 降 低 | C. | 不变 | D. | 无法确定 |
分析 某金属的硝酸盐受热分解生成NO2、O2和某金属氧化物,氮元素化合价由+5价降低为+4价,氧元素化合价由-2价升高为0价,根据NO2和 O2的物质的量之比为8:1,计算氮原子得到的电子、氧原子失去的电子.根据电子转移守恒,判断金属元素化合价变化.
解答 解:某金属的硝酸盐受热分解生成NO2、O2和某金属氧化物,氮元素化合价由+5价降低为+4价,氧元素化合价由-2价升高为0价,生成的二氧化氮和氧气的物质的量之比为8:1,令NO2和 O2的物质的量分别为8mol、1mol,氮原子得到的电子物质的量为8mol×(5-4)=8mol,氧原子失去的电子为1mol×2×[0-(-2)]=4mol.二者氮原子得到的电子大于氧原子失去的电子,根据电子转移守恒,金属原子应提供电子,所以金属元素化合价升高.
故选:A.
点评 考查氧化还原反应的计算,难度不大,根据电子转移守恒判断是关键.注意守恒思想的应用.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 其中氧化剂是MnO2,氧化产物是Cl2,氧化剂和还原剂物质的量之比是1:2.
其中氧化剂是MnO2,氧化产物是Cl2,氧化剂和还原剂物质的量之比是1:2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属的电化学腐蚀比化学腐蚀更普遍 | |
| B. | 在铁板表面涂抹油漆,不能防止铁板被腐蚀 | |
| C. | 钢铁在干燥空气中不易被腐蚀 | |
| D. | 用牺牲锌块的方法来保护船身 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
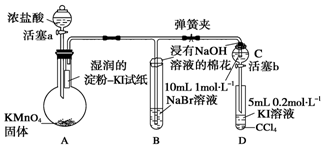
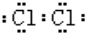 ;A中发生的反应的化学反应方程式为2KMnO4+16HCl═5Cl2↑+2MnCl2+2KCl+8H2O.
;A中发生的反应的化学反应方程式为2KMnO4+16HCl═5Cl2↑+2MnCl2+2KCl+8H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ②③④ | C. | ②③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com