
ŃĒĮņĖįÄĘ(Na2SO3)”¢ĘÆ°×Ņŗ(NaClO)ŗĶĆ÷·Æ[KAl(SO4)2∙12H2O]¶¼ŹĒÖŲŅŖµÄ»Æ¹¤²śĘ·£¬ŌŚČÕ³£Éś»īŗĶ¹¤ŅµÉś²śÖŠ¶¼ÓŠ¹ć·ŗÓĆĶ¾£¬ĒŅČżÕ߶¼æÉÓĆŌŚŌģÖ½ŅµµÄ²»Ķ¬Éś²ś¹¤ŠņÖŠ”£
£Ø1£© NaClO×öĻū¶¾ŅŗŹĒĖüÄÜÓėĖ®·“Ó¦²śÉśŅ»ÖÖĒæŃõ»ÆŠŌĪļÖŹ£¬Š“³öøĆĒæŃõ»ÆŠŌĪļÖŹµÄµē×ÓŹ½_______”£ŌŚ¹¤ŅµÉĻ£¬ÓĆĀČ»ÆÄĘĪŖŌĮĻ£¬ŌŚ¼īŠŌČÜŅŗÖŠ£¬Ķعżµē½āµÄ·½·ØæÉÖʵĆNaClO£¬ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾ÖĘČ”NaClOµÄµē½ā×Ü·“Ó¦£ŗ____________”£½«µČÅØ¶ČµČĢå»żµÄNaClOÓėNa2SO3ČÜŅŗ»ģŗĻŗó£¬Į½ÕßĒ”ŗĆĶźČ«·“Ó¦£¬Š“³ö»ģŗĻ¹ż³ĢµÄĄė×Ó·“Ó¦·½³ĢŹ½ ____________”£
£Ø2£©½«±„ŗĶNaClOŗĶKAl(SO4)2ČÜŅŗ»ģŗĻ£¬ÖĆÓŚŅ»Ö»“ųµ„æ×ĻšĘ¤ČūµÄ“óŹŌ¹ÜÖŠ£¬²śÉś“óĮæµÄ°×É«½ŗד³Įµķ”£“ĖŹ±·“Ó¦µÄĄė×Ó·½³ĢĪŖ____________”£ŌŁ½«“óŹŌ¹ÜÖĆÓŚŃō¹āĻĀÕÕÉ䣬²»¾ĆŹŌ¹ÜŅŗĆęÉĻ·½ÓŠĒ³»ĘĀĢÉ«ĘųĢå²śÉś£¬½«ĘųĢåĶØČėNaOHČÜŅŗ³ä·ÖĪüŹÕŗ󣬻¹ÄÜŹÕ¼Æµ½Ņ»ÖÖĪŽÉ«ĪŽĪ¶µÄĘųĢ唣Š“³öŌŚŃō¹āÕÕÉäĻĀ£¬»ģŗĻŅŗÖŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½____________”£
Čō½«KAl(SO4)2ČÜŅŗ»»³ÉĮņĖįŃĒĢśļ§”¾(NH4)2SO4∙FeSO4”æČÜŅŗŗó£¬ŌŁÓėNaClOČÜŅŗ»ģŗĻ£¬¹Ū²ģµ½“óŹŌ¹ÜÖŠÓŠŗģŗÖÉ«³Įµķ²śÉś£¬Ķ¬Ź±ČÜŅŗĄļĻÖ»ĘÉ«£¬µ«Ć»ÓŠĘųĢåÉś³É”£“ĖŹ±ŹŌ¹ÜÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______”£
£Ø3£©Č”Ņ»¶ØĢå»żKAl(SO4)2ČÜŅŗÓŚŹŌ¹ÜÖŠ£¬ÖšµĪ¼ÓČėŅ»¶ØÅØ¶ČµÄBa(OH)2ČÜŅŗ£¬ Ö±ÖĮ²śÉś³ĮµķµÄÖŹĮæ×ī“󣬊“³ö“ĖŹ±µÄĄė×Ó·“Ó¦·½³ĢŹ½____________”£
 Ó¦ÓĆĢāĢģĢģĮ·ĖÄ“Ø“óѧ³ö°ęÉēĻµĮŠ“š°ø
Ó¦ÓĆĢāĢģĢģĮ·ĖÄ“Ø“óѧ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠČÜŅŗÖŠc(Cl-) Óė50mL 1mol/L ĀČ»ÆĀĮČÜŅŗÖŠµÄc(Cl-) ĻąµČµÄŹĒ
A£®150 mL 1mol/LĀČ»ÆÄĘČÜŅŗ B£®75 mL 2mol/LĀČ»Æļ§ČÜŅŗ
C£®150 mL 1mol/LĀČ»ÆĢśČÜŅŗ D£®75 mL 1mol/LĀČ»ÆŃĒĢśČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬Ķ¬Ģå»żµÄN2ŗĶSO2·Ö×ÓŹżÖ®±ČĪŖ £¬ĪļÖŹµÄĮæÖ®±ČĪŖ £¬Ō×Ó×ÜŹżÖ®±ČĪŖ £¬Ä¦¶ūÖŹĮæÖ®±ČĪŖ £¬ÖŹĮæÖ®±ČĪŖ £¬ĆܶČÖ®±ČĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ£¬pH=1µÄijČÜŅŗAÖŠ»¹ŗ¬ÓŠNH4+”¢K+”¢Na+”¢Fe3+”¢Al3+”¢Fe2+”¢CO32-”¢NO3-”¢Cl-”¢I-”¢SO42£ÖŠµÄ4ÖÖ£¬ĒŅø÷Ąė×ÓµÄĪļÖŹµÄĮæÅØ¶Č¾łĪŖ0.1mol/L£¬ĻÖČ”øĆČÜŅŗ½ųŠŠÓŠ¹ŲŹµŃ飬ŹµŃé½į¹ūČēĻĀĶ¼ĖłŹ¾£ŗ
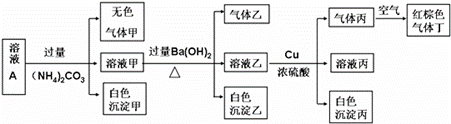
ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ( )
A£®³ĮµķŅŅŅ»¶ØÓŠBaCO3£¬æÉÄÜÓŠBaSO4
B£®ŹµŃéĻūŗÄCu 14.4 g£¬ŌņÉś³ÉĘųĢå±ūĪŖ3.36L
C£®øĆČÜŅŗAÖŠŅ»¶ØÓŠNO3-”¢Al3+”¢SO42£”¢Cl-
D£®Éś³ÉµÄ¼×”¢ŅŅ”¢±ūĘųĢå¾łĪŖĪŽÉ«µÄŅ×ČÜÓŚĖ®ĘųĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¶ŌĻĀĮŠµē½āÖŹČÜŅŗµÄŠšŹö“ķĪóµÄŹĒ£Ø””””£©
”” A£® µČĪļÖŹµÄĮæÅØ¶ČµÄNa2CO3ŗĶNaHCO3»ģŗĻŅŗÖŠ£ŗ
c£ØNa+£©£¾c£ØHCO3﹣£©£¾c£ØCO32﹣£©£¾c£ØOH﹣£©£¾c£ØH+£©
”” B£® 25”ꏱ 0.2 mol•L﹣1ŃĪĖįÓėµČĢå»ż0.05 mol£®L﹣1Ba£ØOH£©2ČÜŅŗ»ģŗĻŗó£¬ČÜŅŗµÄpH=l
”” C£® 25”ꏱ£¬pH=3µÄ¶žŌŖČõĖįH2RČÜŅŗÓėpH=llµÄNaOHČÜŅŗ»ģŗĻŗ󣬻ģŗĻŅŗµÄpHµČÓŚ7£¬Ōņ·“Ó¦ŗóµÄ»ģŗĻŅŗÖŠ£ŗ2c£ØR2﹣£©+c£ØHR﹣£©=c£ØNa+£©
”” D£® 25”ꏱ£¬Čō0.3 mol£®L﹣1 HYČÜŅŗÓė0.3 mol£®L﹣lNaOHČÜŅŗµČĢå»ż»ģŗĻŗó£¬ČÜŅŗµÄpH=9£¬Ōņ£ŗc£ØOH﹣£©﹣c£ØHY£©=1”ĮlO﹣9 mol£®L﹣1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijӊ»śĪļ½į¹¹¼ņŹ½ĪŖ £¬¹ŲÓŚøĆÓŠ»śĪļŠšŹö“ķĪóµÄŹĒ
£¬¹ŲÓŚøĆÓŠ»śĪļŠšŹö“ķĪóµÄŹĒ
A£®1 moløĆĪļÖŹŌŚ¼ÓČČŗĶ“߻ƼĮ×÷ÓĆĻĀ£¬×ī¶ąÄÜŗĶ4 mol H2·¢Éś¼Ó³É·“Ó¦
B£®ÄÜŹ¹äåĖ®ĶŹÉ«Ņ²ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«
C£®ŌŚŅ»¶ØĢõ¼žĻĀ£¬ÄÜ·¢ÉśČ”“ś·“Ó¦
D£®ÓöĻõĖįŅųČÜŅŗ²śÉś°×É«³Įµķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚt”ꏱ£¬½«a gNH3ĶźČ«ČÜÓŚĖ®£¬µĆµ½VmLČÜŅŗ£¬¼ŁÉčøĆČÜŅŗµÄĆܶČĪŖ¦Ńg/mL£¬ÖŹĮæ·ÖŹżĪŖ¦Ų£¬ĘäÖŠŗ¬NH4+µÄĪļÖŹµÄĮæĪŖbmol”£ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø £©
A£®ČÜÖŹµÄÖŹĮæ·ÖŹż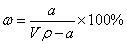
B£®ČÜÖŹµÄĪļÖŹµÄĮæÅضČ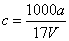 mol/L
mol/L
C£®ČÜŅŗÖŠ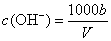 mol/L
mol/L
D£®ĢāŹöČÜŅŗÖŠŌŁ¼ÓČėVmLĖ®ŗó£¬ĖłµĆČÜŅŗµÄÖŹĮæ·ÖŹż“óÓŚ0.5¦Ų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ČōABnŠĶ·Ö×ÓµÄÖŠŠÄŌ×ÓAÉĻƻӊĪ“ÓĆÓŚŠĪ³É¹²¼Ū¼üµÄ¹Ā¶Ōµē×Ó£¬ŌĖÓĆ¼Ū²ćµē×Ó¶Ō»„³āÄ£ŠĶ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®Čōn=2£¬Ōņ·Ö×ÓµÄĮ¢Ģå¹¹ŠĶĪŖVŠĪ””””””
B£®Čōn=3£¬Ōņ·Ö×ÓµÄĮ¢Ģå¹¹ŠĶĪŖČż½Ē׶ŠĪ
C£®Čōn=4£¬Ōņ·Ö×ÓµÄĮ¢Ģå¹¹ŠĶĪŖÕżĖÄĆęĢåŠĪ””””””
D£®ŅŌÉĻĖµ·Ø¶¼²»ÕżČ·
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷×é»ģŗĻĪļÖŠÄܹ»Ź¹ÓĆ·ÖŅŗĀ©¶··ÖĄėµÄŹĒ£Ø””””£©
| ”” | A£® | ±½ŗĶĖ® | B£® | ŅŅ“¼ŗĶŅŅĖį |
| ”” | C£® | ŅŅĖįŗĶŅŅĖįŅŅõ„ | D£® | ĘūÓĶŗĶ²ńÓĶ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com