

| A. | 放电时,锂为负极,发生还原反应 | |
| B. | 充电时阳极反应式为:8Li2S-16e-═S8+16Li+ | |
| C. | 电解质可采用导电有机电解质 | |
| D. | 锂硫电池的理论电压为2.0V,则单位质量的单质硫的比能量为3.35 kW•h/kg |
分析 A.负极发生氧化反应;
B.充电时阳极发生氧化反应,Li2S被氧化生成S;
C.Li与水反应,电解质不能为水溶液;
D.根据Q=UI计算.
解答 解:A.放电时,锂为负极,负极发生氧化反应,故A错误;
B.充电时阳极发生氧化反应,Li2S被氧化生成S,电极方程式为8Li2S-16e-═S8+16Li+,故B正确;
C.Li与水反应,电解质不能为水溶液,可为能导电的有机电解质,故C正确;
D.Q=UI=$\frac{1675mAh/g×2.0V}{1000}$=3.35 kW•h/kg,故D正确.
故选A.
点评 本题考查化学电源新型电池,为高频考点,明确化学电源中各个电极上发生的反应是解本题关键,难点是电极反应式的书写,也为易错点.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 在c(H+)=10-100.1 mol•L-1的溶液中:Al3+、NH4+、Cl-、NO3- | |
| B. | 澄清透明的溶液:Fe2+、Na+、SO42-、NO3- | |
| C. | 水电离出来的c(H+)=10-12 0.1 mol•L-1的溶液:K+、HCO3-、Cl-、ClO- | |
| D. | 能使蓝色石蕊试纸变为红色的溶液:K+、CO32-、Na+、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合溶液中c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) | |
| B. | 混合溶液中c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) | |
| C. | 加入AgNO3溶液时首先生成AgCl沉淀 | |
| D. | 混合溶液中$\frac{c(C{l}^{-})}{c({I}^{-})}$的值约为1.02×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种物质所含原子个数之比为4:3 | |
| B. | 两种物质与水充分反应,生成的氢氧化钠质量之比为2:1 | |
| C. | 两种物质与足量的CO2反应,消耗气体的质量比为1:1 | |
| D. | 两种物质中阳离子的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ③④⑤⑥ | C. | ②③④⑤ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
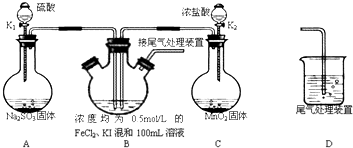 某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:SO2>I->Fe2+,用如图所示装置进行实验(加热和夹持装置已略,气密性已检验).
某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:SO2>I->Fe2+,用如图所示装置进行实验(加热和夹持装置已略,气密性已检验).查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com