

分析 (1)根据装置图分析;根据题给信息易溶于水,难溶于乙醇来解答;
(2)根据硫代硫酸钠遇酸反应生成硫、二氧化硫和水;
(3)根据题目信息SO2、Na2S和Na2CO3反应生成Na2S2O3,结合质量守恒确定产物并配平;
(4)加入盐酸,Na2S2O3反应生成S沉淀,静置后取上层清液,滴加BaCl2溶液,检验溶液中是否含有硫酸根离子;
(5)根据图示的滴定管中液面读出初读数、终读数,然后计算出消耗碘的标准溶液体积,根据反应2S2O32-+I2═S4O62-+2I-可知,n(S2O32-)=2n(I2),然后碘单质的物质的量计算出Na2S2O3•5H2O质量及产品的纯度;
(6)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,反应生成硫酸钠、氯化钠,配平离子方程式.
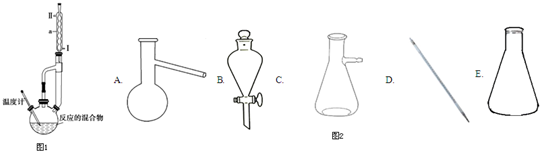
解答 解:(1)根据仪器A的结构特点知A的名称为蒸馏烧瓶;根据题给信息易溶于水,难溶于乙醇,步骤 ④中洗涤时,为了减少产物的损失用的试剂可以是乙醇;
故答案为:蒸馏烧瓶;乙醇;
(2)Na2S2O3在酸性条件下会生成S和二氧化硫,所以产率会下降,其反应的离子方程式为:S2O32-+2H+=S↓+H2O+SO2↑;
故答案为:S2O32-+2H+=S↓+SO2↑+H2O;
(3)三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式为:4SO2+2Na2S+Na2CO3=CO2+3Na2S2O3;
故答案为:4SO2+2Na2S+Na2CO3=CO2+3Na2S2O3;
(4)检测产品中是否存在Na2SO4的实验方案为:取少量产品溶于足量稀盐酸、静置、取上层清液滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质;
故答案为:取少量产品溶于足量稀盐酸、静置、取上层清液滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质;
(5)根据滴定起始和终点的液面位置判断消耗碘的标准溶液体积为18.50mL-2.50mL=16.00mL,n(I2)=0.100 0mol•L-1×0.0016L=1.6×10-4mol,根据2S2O32-+I2═S4O62-+2I-可知知n(Na2S2O3•5H2O)=3.2×10-4mol,m(Na2S2O3•5H2O)=0.7936g,产品的纯度为$\frac{0.7936g}{1.00g}$×100%=79.36%;
故答案为:16.00;79.36%;
(6)Na2S2O3常用作脱氯剂,在溶液中易被Cl2氧化成SO42-,该反应的离子方程式为:S2O32?+4Cl2+5H2O=2SO42?+8Cl?+10H+;
故答案为:S2O32?+4Cl2+5H2O=2SO42?+8Cl?+10H+.
点评 本题考查实验方案方案,涉及仪器识别、对操作的分析评价、方程式书写、离子检验、化学计算等,侧重实验分析能力及知识综合应用能力的考查,题目难度中等.


科目:高中化学 来源:2017届江苏省高三上学期月考一化学试卷(解析版) 题型:选择题
工业上曾经通过反应“3Fe+4NaOH Fe3O4+2H2↑十4Na↑;”生产金属钠。下列有关说法正确的是
Fe3O4+2H2↑十4Na↑;”生产金属钠。下列有关说法正确的是
A.用磁铁可以将Fe与Fe3O4分离
B.将生成的气体在空气中冷却可获得钠
C.该反应条件下铁的氧化性比钠强
D.每生成1molH2,转移的电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 对叔丁基苯酚(
对叔丁基苯酚( )工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚.实验步骤如下:
)工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚.实验步骤如下: .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 相对分 子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解性 | |
| 冬青油 | 152 | 1.180 | 222.2 | 微溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 原子半径大小比较为A>B>C>D | B. | 生成的氢化物稳定性为A>B>C>D | ||
| C. | A与C形成的阴离子可能有AC${\;}_{3}^{2-}$ | D. | A、B、C、D的单质常温下均不导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  反应Ⅰ:△H>0,P2>P1 | B. |  反应Ⅱ:△H<0,T1<T2 | ||
| C. | 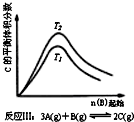 反应Ⅲ:△H<0,T2>T1;或△H>0,T2<T1 | D. | 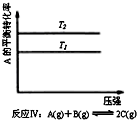 反应Ⅳ:△H<0,T2<T1或△H>0,T2>T1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com