
| A. | 降低温度 | B. | 增大容器体积 | C. | 升高温度 | D. | 选用高效催化剂 |
分析 该反应是一个反应前后气体体积不变的可逆反应,增大压强、升高温度、增大物质浓度、加入催化剂等都能知道反应速率,据此分析解答.
解答 解:该反应是一个反应前后气体体积不变的可逆反应,增大压强、升高温度、增大物质浓度、加入催化剂等都能知道反应速率,
A.降低温度,减少活化分子百分数,所以反应速率减小,故A错误;
B.增大容器体积,单位体积内活化分子数减少,反应速率减小,故B错误;
C.升高温度,增大活化分子百分数,所以反应速率增大,故C正确;
D.选用高效催化剂,降低活化能,增大单位体积内活化分子百分数,反应速率增大,故D正确;
故选CD.
点评 本题考查化学反应速率影响因素,明确化学反应速率影响原理是解本题关键,但外界只是影响因素,物质本身性质决定反应速率.


科目:高中化学 来源: 题型:选择题
| A. | 铜锌原电池中铜是正极 | |
| B. | 在镀件上镀铜时可用金属铜作阳极 | |
| C. | 用电解法精炼铜时粗铜做阳极 | |
| D. | 在电解饱和食盐水的装置可用铜做阳极,且电极产物是Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
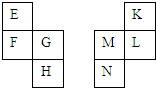 E~N等元素在周期表中的相对位置如下表.E与K的原子序数相差4,K的一种单质是空气中含量最多的物质,H与N属同周期元素,下列判断不正确的是( )
E~N等元素在周期表中的相对位置如下表.E与K的原子序数相差4,K的一种单质是空气中含量最多的物质,H与N属同周期元素,下列判断不正确的是( )| A. | 原子半径:M>L>K | |
| B. | F的单质与氧气反应只生成一种氧化物 | |
| C. | H与N的原子核外电子数相差14 | |
| D. | 最高价氧化物的水化物酸性:K>L>M |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 机身隔框一般采用超硬铝,承受较大载荷的加强框采用高强度结构钢或钛合金 | |
| B. | 航空发动机对材料的要求非常高,所以其气缸必须使用纯度相当高的金属材料 | |
| C. | 很多飞机的机载雷达装在机身头部,一般采用玻璃纤维增强塑料做成的头锥将机身头部罩住以便能透过电磁波 | |
| D. | 采用特殊的新型复合材料作为表面涂层,使其几乎不反射雷达所发出的电磁波,雷达就检测不到 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24 L CO2中含有的原子数为0.3×6.02×1023 | |
| B. | 0.1 L 3 mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 4.5 g SiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 | |
| B. | 进行分液时,分液漏斗中的下层液体,从下端流出,上层液体则从上口倒出 | |
| C. | 萃取、分液前需对分液漏斗进行检漏 | |
| D. | 将上面的塞子拿下,可以保证分液漏斗内的液体顺利流出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
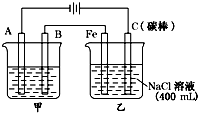 如图为相互串联的甲乙两电解池.试回答:
如图为相互串联的甲乙两电解池.试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com