
分析 (1)乙烯中含有碳碳双键,性质较活泼,能发生加成反应;
(2)光照条件下,烷烃和氯气能发生取代反应生产氯代烃;
(3)乙烯中含有碳碳双键,性质较活泼,能被强氧化剂氧化.
解答 解:(1)乙烯中含有碳碳双键,性质较活泼,能和溴发生加成反应生成1,2-二溴乙烷,该反应为加成反应,故选C;
(2)光照条件下,烷烃和氯气能发生取代反应生产氯代烃,则光照条件下甲烷和氯气发生取代反应生成氯代烃,该反应为取代反应,故选A;
(3)乙烯中含有碳碳双键,性质较活泼,能被强氧化剂酸性高锰酸钾溶液氧化生成二氧化碳,该反应为氧化反应,故选B.
点评 本题考查有机物结构和性质、有机反应类型判断,为高频考点,明确官能团及其性质关系是解本题关键,知道常见反应类型与官能团的关系、常见反应条件,题目难度不大.


科目:高中化学 来源: 题型:解答题
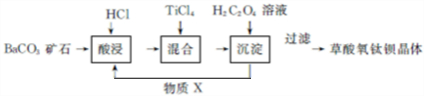
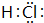 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:正戊烷>2-甲基丁烷>丙烷 | |
| B. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| C. | 相对分子质量相近的醇比烷烃沸点高是因为醇分子间存在氢键 | |
| D. | 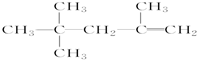 的名称为2,2,4-三甲基-4-戊烯 的名称为2,2,4-三甲基-4-戊烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 风能是人类通过风车等工具获取的能源,但属于一次能源 | |
| B. | 在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源 | |
| C. | 月球土壤中含有丰富的质量数为3的氦,它可作为未来核能的重要原料 | |
| D. | 原电池把化学能直接转化为电能,所以由原电池提供的电能是一次能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和稀硫酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 向硫酸钠溶液中滴加氯化钡溶液 Ba2++SO42-═BaSO4↓ | |
| C. | 氯水加入到溴化钾溶液中 Br-+Cl2═Br2+Cl- | |
| D. | 碳酸钙溶于稀盐酸 CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
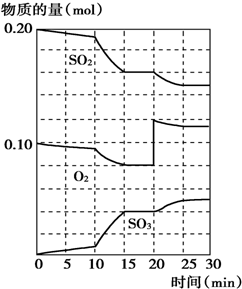
| A. | .反应从0min开始,到第一次平衡时,二氧化硫的转化率为40% | |
| B. | 反应进行到10min至15min时,曲线发生变化可能是因为升高了温度 | |
| C. | 反应进行至20min时,曲线发生变化是因为通入了氧气 | |
| D. | 在15min~20min、25min~30min内时反应处于平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
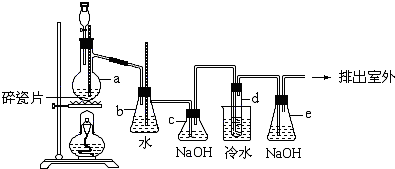
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
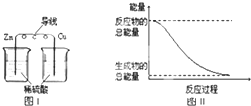
| A. | 化学反应中能量变化的主要原因是物质状态的改变 | |
| B. | 铝热反应中,反应物的总能量比生成物的总能量高 | |
| C. | 图I所示的装置能将化学能转变为电能 | |
| D. | 图II所示的反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解水产生氢气 | |
| B. | 开发特殊物质作催化剂,降低水分解过程中所需要的能量 | |
| C. | 大量建设水电站,用电力分解水制取氢气 | |
| D. | 寻找更多化石燃料,利用燃烧放热,使水分解产生氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com