
| A. | 若混合物为Zn、Al,w不可能是0.1mol | |
| B. | 若混合物为Zn、Fe,w可能大于0.1mol | |
| C. | 若混合物为Fe、Mg,则加入的稀硫酸中溶质质量分数等于9.8% | |
| D. | 若混合物为Cu、Fe,w是0.05mol,则混合物中Fe与Cu的质量比为1:1 |
分析 A.根据反应方程式利用极值法进行计算;
B.根据铁、锌与稀硫酸反应的方程式利用极值法分析;
C.镁和稀硫酸反应生成硫酸镁和氢气;
D.铜不与稀硫酸反应,根据反应方程式计算出铁的质量,然后计算出二者质量比.
解答 解:A.锌、铝和稀硫酸反应的化学方程式及其质的量关系为:Zn+H2SO4═ZnSO4+H2↑,2Al+3H2SO4═Al2(SO4)3+3H2↑,
65g 1mol 54g 3mol
由以上关系可知,5.6g锌和稀硫酸恰好完全反应生成的氢气小于0.1mol,5.6g铝和稀硫酸恰好完全反应生成的氢气大于0.1mol,因此若混合物为Zn、Al,w可能是0.1mol,故A错误;
B.铁和稀硫酸反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑,
56g 1mol,
5.6g铁和稀硫酸恰好完全反应生成的氢气的物质的量为0.1mol,由A中可知,5.6g锌和稀硫酸恰好完全反应生成的氢气小于0.1mol,因此若混合物为Fe、Zn,w一定小于0.1mol,w不可能大于0.1mol,故B错误;
C.设5.6g铁消耗硫酸的质量为y,5.6g镁消耗硫酸的质量为z,
Fe+H2SO4═FeSO4+H2↑,Mg+H2SO4═MgSO4+H2↑,
56 98 24 98
5.6g y 5.6g z
则:$\frac{56}{5.6g}$=$\frac{98}{y}$,$\frac{24}{5.6g}$=$\frac{98}{z}$,
y=9.8g,z=22.9g,
则加入的稀硫酸中溶质质量分数最小为:$\frac{9.8g}{100g}$×100%=9.8%,稀硫酸中溶质的最大质量分数为:$\frac{22.9g}{100g}$×100%=22.9%,所以该硫酸的质量分数一定大于9.8%,故C错误;
D.设铁的质量为x,
Fe+H2SO4═FeSO4+H2↑,
56g 1mol
x 0.05mol
则:$\frac{56g}{x}=\frac{1mol}{0.05mol}$,
解得:x=2.8g,
则混合物中Fe和Cu的质量比为:2.8g:(5.6g-2.8g)=1:1,故D正确;
故选D.
点评 本题考查混合物反应的计算,题目难度中等,试题侧重考查学生运用假设法和化学方程式进行计算和推断的能力,试题培养了学生的分析能力及化学计算能力.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | Z | M | |
| A | N2 | NO | NO2 | O2 |
| B | Cl2 | FeCl3 | FeCl2 | Fe |
| C | Al2O3 | NaAlO2 | Al(OH)3 | NaOH |
| D | S | SO2 | SO3 | O2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,其结构和物理性质和苯相似,称为“无机苯”,该物质的二氯代物有4种.
,其结构和物理性质和苯相似,称为“无机苯”,该物质的二氯代物有4种.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:| 元 素 | Mn | Fe | |
| 电离能 /kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
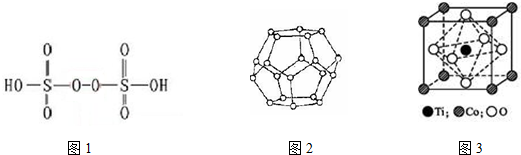
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com