




| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
 2MgO����3Mg+N2
2MgO����3Mg+N2 Mg3N2����2Mg+CO2
Mg3N2����2Mg+CO2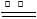 2MgO+C��
2MgO+C�� MgO+H2���� ��Mg3N2 +6H2O
MgO+H2���� ��Mg3N2 +6H2O 3Mg(OH)2+2NH3��
3Mg(OH)2+2NH3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
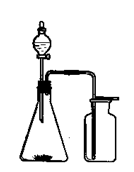
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
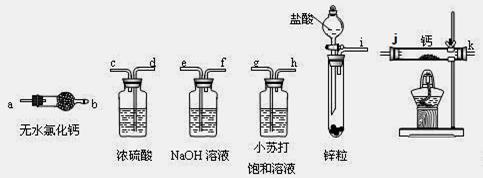
| A�����ȷ�Ӧһ��ʱ�� | B���ռ����岢�����䴿�� |
| C���رշ�Һ©������ | D��ֹͣ���ȣ������ȴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
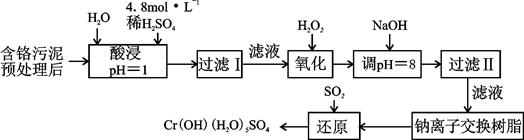
| ������ | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| ��ʼ����ʱ��pH | 1.9 | 7.0 | ���� | ���� | 4.7 | ���� |
| ������ȫʱ��pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 ����9�ܽ⣩ |
 Cr3+(aq)+3OH��(aq)
Cr3+(aq)+3OH��(aq)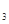 ���ܶȻ�Ksp= c(Cr3+)? c3(OH��)=10��32��Ҫʹc(Cr3+)����10��5mol/L����Һ��pHӦ���� ��
���ܶȻ�Ksp= c(Cr3+)? c3(OH��)=10��32��Ҫʹc(Cr3+)����10��5mol/L����Һ��pHӦ���� ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| ��� | ʵ�鷽�� | ʵ������ͽ��� |
| ����1 | ȡ������Ʒ | ��Ʒ��ɫ�����б仯�� |
| ����2 | ����1����Ʒת�Ƶ��Թ��У�����ȥ������ˮ�����ܽ⣬���������ԣ�________ ___________ __ �� | �� ��˵����Ʒ�к���FeSO4��7H2O���ʡ� |
| ����3 | ������2֤����Ʒ����FeSO4?7H2O���ʣ�����ȡ��Ʒ�ⶨ����NH4+����������w1������ֵw2�Ƚϡ� | ��w1 w2��˵����Ʒ�к��У�NH4)2SO4���ʡ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��SO2 | B��NH3 | C��N2 | D��CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
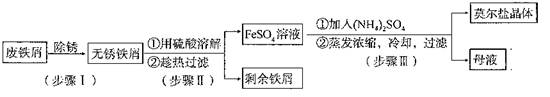
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
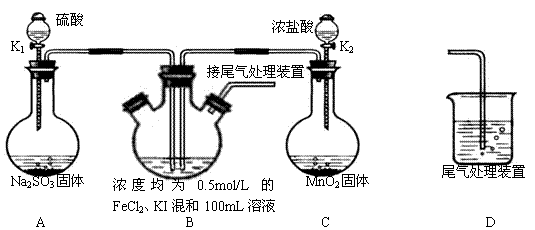
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com