
【题目】浓度不等的两种硫酸溶液等质量混合后,溶液的质量分数为a%,而等体积混合后,溶质的质量分数为 b%;浓度不等的两种氨水等质量混合后,溶液的质量分数为a%,而等体积混合后,溶质的质量分数为c%,那么,a、b、c数值的关系是( )
A.b>a>c
B.c>a>b
C.c>b>a
D.a>b>c
【答案】A
【解析】解:假设两种溶液的质量分数分别是x y,其中x<y,
对于硫酸溶液,
等质量(假设都是m g)混合之后,混合溶液质量分数= ![]() =
= ![]() ,
,
等体积混合时,由于质量分数小的硫酸密度比较小,等体积的两种硫酸,质量分数大的质量大,那么等体积混合相当于先将二者等质量混合,然后再加入一定量的高质量分数组分的硫酸,因此混合溶液质量分数> ![]() ;
;
同样,对于氨水溶液,
等质量混合时其浓度依然是 ![]() ,
,
等体积混合时,由于质量分数小的氨水溶液密度比较大(因为氨水的密度比水小),等体积的两种氨水溶液,质量分数大的质量小,那么等体积混合相当于先将二者等质量混合,然后再加入一定量的低质量分数组分的氨水溶液,因此混合溶液质量分数< ![]() .
.
则有b>a>c,
故选A.


科目:高中化学 来源: 题型:
【题目】将0.03mol Cl2缓缓通入含0.02mol H2SO3和0.02mol HBr的混合溶液中,在此过程溶液的c(H+)与Cl2用量的关系示意图是(溶液的体积视为不变)( )
A.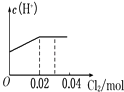
B.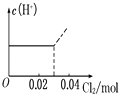
C.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)在实验室中,常使气体通过干燥剂①浓硫酸②碱石灰,达到干燥气体的目的.干燥下列气体可选择所列出的哪种干燥剂(填序号) SO2NH3Cl2
(2)在氮的单质和常见化合物中: 常用作保护气(如填充灯泡)的物质是 , 常用作制冷剂的物质是 .
(3)舍勒将软锰矿与浓盐酸混合加热,在世界上首先制得了氯气.反应的离子方程式为: .其中,氧化剂是 . 高锰酸钾是强氧化剂,用高锰酸钾与浓盐酸混合在常温下即可反应生成氯气,从反应条件分析,高锰酸钾与二氧化锰谁的氧化性更强? .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学已经渗透到人类生活的各个方面,下列说法正确的是
A.垃圾焚烧不仅可以用于发电,还不会带来任何新污染
B.喂养鸡的过程中大量使用抗生素,大量进食这样的鸡肉对人体健康有益
C.油脂在人体内水解为氨基酸和甘油等小分子被吸收
D.铜具有良好的导电性,常用来制作印刷电路板
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢是一种应用范围极广的过氧化物,根据题意,回答下列有关问题:
(1)请举出H2O2的一种用途 .
(2)H2O2是一种二元弱酸,请写出它的第一步电离方程式 .
(3)将H2O2溶液加入盐酸酸化的FeCl2溶液中,溶液由浅绿色变为棕黄色,写出该反应的离子方程式并标出电子转移情况 .
(4)向盛有少量过氧化钠固体的试管中滴加水,直到气体不再放出,再加水稀释所得溶液,将得到的溶液平均分成两份盛放在两只试管中,进行下列实验:①一只试管中滴加酚酞试液,溶液变红.半分钟红色褪去;②另一只试管中加入少量二氧化锰.又有气体放出,待气体不再放出,再滴加酚酞,溶液变红,持久不褪色.上述实验表明,过氧化钠和水反应可分两步,其化学方程式为: 第一步:;第二步 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.水的摩尔质量是18 gmol﹣1
B.硫离子的结构示意图: ![]()
C.8个质子、10个中子的原子: ![]() O
O
D.四氯化硅中Si的化合价为﹣4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)碱式氯化铜是重要的无机杀菌剂.
(1)碱式氯化铜有多种制备方法
①方法1:45~50℃时,向CuCl悬浊液中持续通入空气得到Cu2 (OH)2 Cl23H2O,该反应的化学方程式为 .
②方法2:先制得CuCl2 , 再与石灰乳反应生成碱式氯化铜.Cu与稀盐酸在持续通入空气的条件下反应生成CuCl2 , Fe3+对该反应有催化作用,其催化原理如图所示. M′的化学式为 . 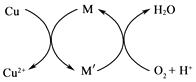
(2)碱式氯化铜有多种组成,可表示为Cua(OH)bClcxH2O. 为测定某碱式氯化铜的组成,进行下列实验:
①称取样品1.1160g,用少量稀HNO3溶解后配成100.00mL溶液A;
②取25.00mL溶液A,加入足量AgNO3溶液,得AgCl 0.1722g;
③另取25.00mL溶液A,调节pH 4~5,用浓度为0.08000molL﹣1的EDTA(Na2H2Y2H2O)标准溶液滴定Cu2+ (离子方程式为Cu2++H2Y2﹣═CuY2﹣+2H+),滴定至终点,消耗标准溶液30.00mL.通过计算确定该样品的化学式(写出计算过程).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com