
| A. | 25℃时,0.1 mol/LHX溶液中pH=1 | |
| B. | Ksp(CaX2)随温度和浓度的变化而变化 | |
| C. | 该体系中,c(Cl-)=c(Ca2+) | |
| D. | 该体系中HX与CaCl2反应产生沉淀 |
分析 A.HX酸为弱酸,溶液中不能完全电离;
B.Ksp只与温度有关;
C.如生成CaX2沉淀,则c(Cl-)>2c(Ca2+);
D.计算c(X-)、c(Ca2+),可确定是否生成沉淀.
解答 解:A.HX酸为弱酸,不能完全电离,则25℃时,0.1 mol•L-1HX溶液中pH>1,故A错误;
B.Ksp只与温度有关,则Ksp(CaX2)随温度的变化而变化,与浓度无关,故B错误;
C.如生成CaX2沉淀,则c(Cl-)>2c(Ca2+),如不生成沉淀,c(Cl-)=2c(Ca2+),故C错误;
D.1L 0.2mol/LHX溶液中加入1L 0.2mol/LCaCl2溶液,混合后c(X-)=$\sqrt{3.6×1{0}^{-5}}$、c(Ca2+)=0.1mol/L,则Qc=c2(X-)•c(Ca2+)=(3.6×10-5mol/L)•0.1 mol•L-1=3.6×10-6>Ksp,说明有沉淀产生,故D正确.
故选D.
点评 本题考查难溶物溶解平衡及溶度积的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,题目难度中等,注意利用溶度积判断沉淀能否生成,把握影响平衡常数的因素即可解答.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 化学反应中,物质变化的同时不一定发生能量变化 | |
| B. | 反应焓变(△H)的大小与方程式中各物质的化学计量系数无关 | |
| C. | 反应产物的总焓大于反应物的总焓时,反应吸热,△H>0 | |
| D. | 吸热反应中,形成化学键释放的能量大于断裂化学键吸收的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤ | B. | ①③⑥ | C. | ②④ | D. | ②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5<pH<7.1 | B. | 7.1<pH<9 | C. | 3<pH<7.1 | D. | 7.1<pH<11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
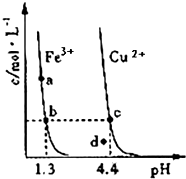 某温度下,将Fe(OH)3(s)、Cu(OH)2(s)分别置于蒸馏水中达到沉淀溶解平衡后,金属阳离子浓度随溶液pH的变化如图所示.下列判断正确的是( )
某温度下,将Fe(OH)3(s)、Cu(OH)2(s)分别置于蒸馏水中达到沉淀溶解平衡后,金属阳离子浓度随溶液pH的变化如图所示.下列判断正确的是( )| A. | 该温度下,Ksp[Fe(OH)3]>Ksp[Cu(OH)2] | |
| B. | c、d 两点代表的溶液中c(H+) 与c(OH-) 乘积不相等 | |
| C. | Cu(OH)2在c点比在d点代表的溶液中溶解程度小 | |
| D. | 加适量浓NH3•H2O可使溶液由a点变到b点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某温度下,Ksp(AgCl)=1.8×10-10,Ksp (Ag2CrO4)=1.9×10-12,故Ag2CrO4更难溶 | |
| B. | 在CaCO3饱和溶液中,加入CaCl2固体,沉淀溶解平衡逆向移动,溶液中Ca2+浓度减小 | |
| C. | 溶度积常数Ksp与温度有关,温度越高,溶度积越大 | |
| D. | 在AgCl饱和溶液中,加入AgCl固体,平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 名称 | 相对分子质量 | 性状 | 熔点 | 沸点 | 密度 | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |
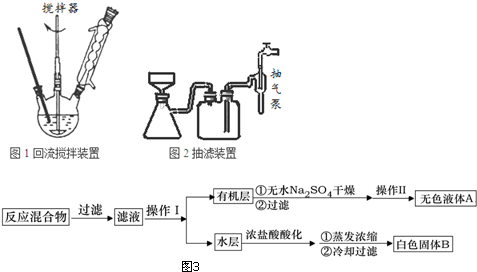
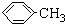 ;操作Ⅱ为蒸馏.
;操作Ⅱ为蒸馏.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
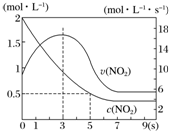 某绝热恒容容器中充入2mol•L-1 NO2,发生反应2NO2(g)═N2O4(g)△H=-56.9kJ•mol-1.下列分析不正确的是( )
某绝热恒容容器中充入2mol•L-1 NO2,发生反应2NO2(g)═N2O4(g)△H=-56.9kJ•mol-1.下列分析不正确的是( )| A. | 5s时NO2的转化率为75% | |
| B. | 0~3 s时v(NO2)增大是由于体系温度升高 | |
| C. | 3s时化学反应处于平衡状态 | |
| D. | 9s时再充入N2O4,平衡后K较第一次平衡时大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C-C | C-H | H-H | C-O | C≡O | O-H |
| 键能/kJ/mol | 348 | 413 | 436 | 358 | x | 463 |
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol/L | 0.5 | 2 | 2 | 0.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com