
| A、3.2ag |
| B、3.2+a g |
| C、(a-3.2)g |
| D、(a-6.4)g |


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
| A、CaCl2和Na2CO3 |
| B、稀H2SO4和NaHCO3 |
| C、Ba(OH)2和NaHCO3 |
| D、NaAlO2和盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.3g钠在空气中加热反应时,失去的电子数为0.2NA |
| B、标准状况下,1.12L的HCHO所含的原子数为0.2NA |
| C、28g C2H4和C4H8混合物中所含的分子数为3NA |
| D、1mol FeCl3与沸水反应生成胶体后,含有NA个Fe(OH)3胶粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该容器中发生了氧化还原反应 |
| B、该反应中HNO3、H2O是反应物,H2SO4、NO、H3AsO4是生成物 |
| C、该反应中只有砷元素被氧化、只有氮元素被还原 |
| D、HNO3、H2SO4、H3AsO4都属于最高价氧化物的水化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ②Na+结构示意图为
②Na+结构示意图为  ③Fe3O4中氧元素的化合价是-2
③Fe3O4中氧元素的化合价是-2 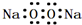 ⑥16O2与18O2互为同分异构体.
⑥16O2与18O2互为同分异构体.| A、①③ | B、③④ | C、②⑤ | D、④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com