
| A��0��4 mol | B��0��6 mol |
| C��0��8 mol | D��0��2 mol |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��N2O | B��NO | C��N2O3 | D��NO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
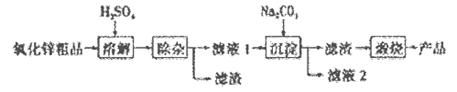
 CoO2��LiC6����ŵ�ʱ����ص�������ӦʽΪ________________����ͼ��ʾ��װ�ù���ʱ���Ӻ����ӵ��ƶ�����ʱ�õ�ش���_________(��ŵ硱��硱)״̬��
CoO2��LiC6����ŵ�ʱ����ص�������ӦʽΪ________________����ͼ��ʾ��װ�ù���ʱ���Ӻ����ӵ��ƶ�����ʱ�õ�ش���_________(��ŵ硱��硱)״̬��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��(a��3b) mol |
B�� |
C�� |
| D��(cV��3a��9b) mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������Ӧ�У�ÿ����2mol NO2���ͻ�����22��4L N2O |
| B��N2O�������ԣ���ΪHNO2������ |
| C����������N2O��CO2������ȵĵ����� |
| D��N2O��Ѹ��������Ѫ�쵰��ϣ�ʹ���ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| A��MnO2 | B��KMnO4��Һ | C��ϡ���� | D��Na2SO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Cu��Cu2O�����ʵ���֮��Ϊ2��1 |
| B����������ʵ���Ũ��Ϊ2.6 mol��L��1 |
| C��������NO�ڱ�״���µ����Ϊ4.48 L |
| D��Cu��Cu2O�����ᷴӦ��ʣ��HNO3Ϊ0.2 mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com