
分析 (1)反应热与反应物的总能量和生成物的总能量,与反应条件无关;
(2)化学键断裂为吸热过程,新键生成放热的过程;
(3)常温时红磷比白磷稳定,说明白磷能量高,反应放出的热量较多;
(4)根据热化学方程式的含义和书写方法来回答;
(5)化学反应的焓变△H=△H=断键吸收的能量-成键放出的能量,结合化学键能和物质能量的关系求解△H2,根据盖斯定律计算H2O2分解反应的焓变.
解答 解:(1)反应热与反应物的总能量和生成物的总能量,与反应条件无关,则光照和点燃条件的△H相同,
故答案为:=;
(2)氢气分子生成氢原子要破坏化学键,需要吸热,则2mol氢原子所具有的能量大于1mol氢分子所具有的能量,
故答案为:>;
(3)常温时红磷比白磷稳定,说明白磷能量高,反应放出的热量较多,因△H<0,则放出的能量越多反应热越小,
故答案为:<;
(4)1molCl2参与反应时释放出145KJ热量,则反应2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)会放出290KJ的能量,即2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290.0 kJ•mol-1,
故答案为:2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290.0 kJ•mol-1;
(5)H-H、O=O和O-H键的键能分别为436kJ/mol、497kJ/mol和462kJ/mol,化学反应的焓变△H=断键吸收的能量-成键放出的能量,1mol水含有2molH-O键,则2H2O(g)═2H2(g)+O2 (g)△H2=(4×462kJ/mol-2×436kJ/mol-497kJ/mol)=+479kJ/mol,①H2(g)+O2(g)═H2O2(l)△H1=-134KJ/mol ②2H2O(g)═2H2(g)+O2 (g)△H2=+479kJ/mol,根据盖斯定律:-[①×2+②]得2H2O2(g)═2H2O(g)+O2(g)△H=-(2×△H1+△H2)=-[2×(-134KJ/mol)+479kJ/mol]=-211kJ/mol,
故答案为:2H2O2(l)=2H2O(g)+O2(g)△H=-211kJ/mol.
点评 本题综合考查反应热的大小比较以及热化学方程式的书写,题目难度不大,注意把握比较反应热的角度.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | ①是非氧化还原反应,而②是氧化还原反应 | |
| B. | 上述反应中SO2的作用只相当于催化剂 | |
| C. | 反应②中CuSO4是氧化产物 | |
| D. | 反应①中SO2发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制CuCl2溶液时,将CuCl2(s)溶于浓HCl后再加水冲稀,浓盐酸作用:有利于抑制CuCl2水解,可防止Cu(OH)2的形成 | |
| B. | 加热MnO2的浓HCl溶液制取氯气.浓盐酸作用:有利于减少氯气的溶解损失 | |
| C. | 浓硝酸不能溶解金,需用浓HCl溶液配制王水才能溶解金.浓盐酸作用:有利于增强Au的还原性,并且提高硝酸的氧化性 | |
| D. | 将浓硫酸滴入浓盐酸中制备HCl气体.浓盐酸作用:增大溶质的浓度,有利于促进平衡向气体溶解的逆方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z | W |
| A. | X、Z、W的简单氢化物的稳定性Z>W>X | |
| B. | X元素的单质在化学反应中只表现还原性 | |
| C. | X、Y的简单离子半径Y>X | |
| D. | Y、Z、X的最高价氧化物均能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某反应由两步反应A═B═C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A═B═C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A. | A═B的反应热△H=+(E2-E1)KJ/mol | B. | 三种化合物中C最稳定 | ||
| C. | C═B 是放热反应 | D. | 整个反应中△H=E1-E4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 有关信息 |
| A | 其氢化物水溶液呈碱性 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
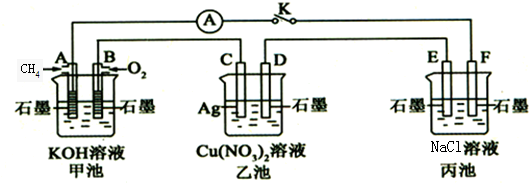
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16种 | B. | 25种 | C. | 36种 | D. | 64种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com