
| A. | 苯和甲苯分子中所有原子均在同一平面上 | |
| B. | 苯不可以使KMnO4酸性溶液褪色而甲苯可以 | |
| C. | 苯和甲苯都能与卤素单质、硝酸等发生取代反应 | |
| D. | 苯的同系物的分子通式是CnH2n-6(n≥7) |
分析 A.甲苯含有甲基,具有甲烷的结构特点;
B.苯性质稳定,但甲苯可被氧化;
C.苯、甲苯在催化条件下可发生取代反应;
D.苯的同系物含有一个苯环,且烃基为烷基.
解答 解:A.苯为平面形结构,但甲苯含有甲基,具有甲烷的结构特点,不可能在同一个平面上,故A错误;
B.苯性质稳定,但甲苯中苯环对甲基的影响,导致甲苯可被氧化,可使高锰酸钾褪色,故B正确;
C.苯、甲苯在催化条件下可发生取代反应,可生成硝基苯、三硝基甲苯等,故C正确;
D.苯的同系物含有一个苯环,且烃基为烷基,通式为CnH2n-6(n≥7),故D正确.
故选A.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重考查学生的分析能力,注意把握有机物的组成、结构和性质,注意有机物的空间结构问题,为易错点,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释或对应的离子方程式 |
| A | 用热的纯碱溶液洗去油污 | Na2CO3可直接和油污反应 |
| B | 酸雨样品在空气中放置pH减小 | 亚硫酸被氧化为硫酸 2H2SO3+O2=2H2SO4 |
| C | “84”消毒液具有漂白性 | ClO-+CO2+H2O=HClO+HCO3- |
| D | 用加热法除去NaCl固体中混有的NH4Cl固体 | NH4Cl固体可以完全分解成为气体而除去 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是在反应②中既是氧化产物又是还原产物 | |
| B. | 氧化性强弱的顺序为:BrO3->ClO3->Cl2>Fe3+ | |
| C. | 溶液中可发生:ClO3-+6Fe2++6H+═Cl-+6Fe3++3H2O | |
| D. | Cl2在①、③反应中均作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 LCH3CH2OH中含有分子的数目为0.5NA | |
| B. | 58.5gNaCl晶体中含有NA个NaCl分子 | |
| C. | 56g铁粉与一定量氯化铁溶液反应生成0.75molFeCl2,失去的电子数为0.5 NA | |
| D. | 100mL浓度均为0.2mol/L的MgCl2和AlCl3混合溶液中阴离子的数目为0.05NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
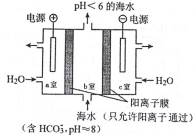 利用如图所示装置从海水中提取CO2,也有利于减少温室气体含量.
利用如图所示装置从海水中提取CO2,也有利于减少温室气体含量.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com