
【题目】高能固氮反应条件苛刻,计算机模拟该历程如图所示,在放电的条件下,微量的O2或N2裂解成游离的O或N原子,分别与N2和O2发生以下连续反应生成NO。下列说法错误的( )
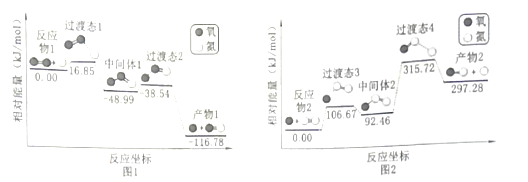
A.图1中,中间体1到产物1的方程式为O-O═N→O+N═O
B.NO的生成速率很慢是因为图2中间体2到过渡态4的能垒较大
C.由O和N2制NO的活化能为315.72kJmol-1
D.由N和O2制NO的过程比由O原子和N2制NO的过程速率慢
【答案】D
【解析】
A、由图1可知,中间体1为O-O═N,产物1为O+N═O,所以中间体1到产物1的方程式为O-O═N→O+N═O,故A正确;
B、反应的能垒越高,反应速率越小,总反应的快慢主要由机理反应慢的一步决定,由图2可知,中间体2到过渡态4的能垒较大、为223.26kJ/mol,决定了NO的生成速率很慢,故B正确;
C、由图2可知,反应物2到过渡态4的能垒为315.72kJmol-1,过渡态4到反应物2放出能量为逆反应的活化能,所以由O和N2制NO的能垒或活化能为315.72kJmol-1,故C正确;
D、由图1可知,N和O2制NO的过程中各步机理反应的能垒不大,反应速率较快;由图2可知,O原子和N2制NO的过程中多步机理反应的能垒较高、中间体2到过渡态4的能垒为223.26kJ/mol,导致O原子和N2制NO的反应速率较慢,所以由N和O2制NO的过程比由O原子和N2制NO的过程速率快,故D错误;
故选:D。


科目:高中化学 来源: 题型:
【题目】一种磁性材料的磨削废料(含镍质量分数约21%)主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物。用该废料制备纯度较高的氢氧化镍,工艺流程如图所示:
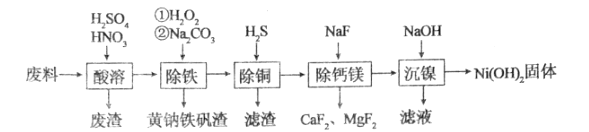
请回答下列问题:
(1)为了提高“酸溶”工序中原料的浸出效率,采取的措施不合理的有______。
A.搅拌
B.适当升高温度
C.研磨矿石
D.用浓硫酸
(2)“酸溶”时,溶液中有Fe3+、Fe2+、Ni2+等生成,废渣的主要成分是______;合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,反应有N2生成,金属镍溶解的离子方程式为______。
(3)“除铁”时控制温度不超过40℃的原因是______;加入碳酸钠的目的是______。
(4)Fe2+也可以用NaClO3氧化,生成的Fe3+在较小pH条件下水解,最终形成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀而被除去,图表示pH-温度关系,图中阴影部分为钠铁矾稳定存在的区域。
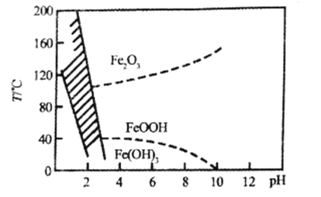
则下列说法不正确的是______(填字母)
a.黄钠铁矾[Na2Fe6(SO4)4(OH)12]中铁为+2价
b.pH过低或过高均不利于生成黄钠铁矾,其原因相同
c.氯酸钠在氧化Fe2+时,1 molNaClO3得到的电子数为6NA
d.工业生产中温度常保持在85℃-95℃,控制溶液的pH为1.2~1.8,此时加入Na2SO4后生成黄钠铁矾
(5)“除铜”时,反应的离子方程式为______,若用Na2S代替H2S除铜,优点是______。
(6)已知某温度下Ksp[Ni(OH)2]=4.0×10-15,该流程在“沉镍”过程中需调节溶液pH约为______,Ni2+才刚好沉淀完全(离子沉淀完全的浓度≤10-5mol/L;lg2=0.30)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠被称为工业盐,在漂白、电镀等方面应用广泛。以木炭、浓硝酸、水、和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如图所示。
已知:室温下,①2NO+Na2O2=2NaNO2
②酸性条件下,NO或NO2—都能与MnO4—反应生成NO3—和Mn2+,5 NO2— + 2MnO4—+ 6H+= 5NO3—+ 2Mn2++ 3H2O
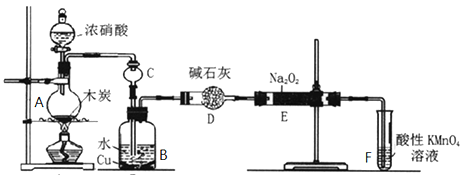
(1)A中观察到的现象__________________________。
(2)装置B中反应的离子方程式有____________________,_____________________。
(3)装置C的作用:____________________,装置F的作用:___________________。
(4)若无装置D,则E中产物除亚硝酸钠外还含有副产物__________________。(填化学式)
(5)NaNO2有像食盐一样的咸味,但能引起中毒。已知亚硝酸钠能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O,根据上述反应,可以用试剂和生活中常见的物质进行实验,以鉴别亚硝酸钠和食盐。进行实验时,必须选用的物质有__________________。
A.自来水 B.碘化钾淀粉试液 C.淀粉 D.白糖 E.食醋 F.白酒
(6)充分反应后,某同学设计实验对E中NaNO2的含量进行检测。称取E中固体2g,完全溶解配制成溶液100 mL,取出25 mL溶液用0.100 mol/L酸性KMnO4溶液进行滴定(杂质不与KMnO4反应),消耗KMnO4溶液20mL,求样品中亚硝酸钠的质量分数(只列式,不用化简,不用计算,已知:NaNO2摩尔质量69g/mol)____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表达式书写正确的是( )
A.NaHCO3的电离方程式:NaHCO3=Na++H++CO32-
B.HS-的水解方程式:HS-+H2O![]() H3O++S2-
H3O++S2-
C.CO32-的水解方程式:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
D.BaSO4的沉淀溶解平衡表达式:BaSO4(s) ![]() Ba2+(aq)+SO42-(aq)
Ba2+(aq)+SO42-(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置,在仪器甲乙丙中,分别依次加入下列各选项中所对应的试剂进行实验。能达到实验目的的是( )
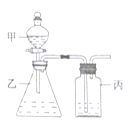
A.浓盐酸、高锰酸钾、浓硫酸,制取纯净的氯气
B.浓盐酸、浓硫酸、浓硫酸,制取干燥的氯化氢气体
C.稀硫酸、溶液X、澄清石灰水,检验溶液X中是否含有碳酸根离子
D.稀硫酸、碳酸钠、次氯酸钠,验证硫酸、碳酸、次氯酸的酸性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫化合物在生活和生产中有着重要应用,科学使用含硫化合物对人体健康及环境保护意义重大。
(1)葡萄酒中添加微量的SO2可抑制细菌生长,防止葡萄酒被__(填“氧化”、“还原”)。
(2)氢的硫化物有多种:H2Sx(x=1,2,3,…),如H2S2,其结构与H2O2相似。请写出H2S3的结构式__。
(3)固体硫酸氢钾在加热熔化时,生成了焦硫酸钾(K2S2O7),反应中断裂的化学键类型为__。
(4)淮北某课题小组对连二亚硫酸钠(Na2S2O4)进行了如下探究。将0.050ml·L-1Na2S2O4溶液在空气中放置,其溶液的pH与时间(t)的关系如图所示(忽略溶液体积的变化)。
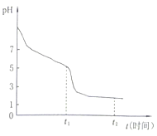
①Na2S2O4溶液显__性,原因是__(用离子方程式表示)。
②t1时溶液中只有一种溶质,此时含硫元素的粒子浓度由大到小的顺序为___。
0-t1段发生反应的离子方程式为__,t1-t2段溶液的pH变小的原因是__(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是
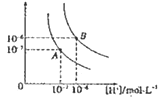
A. 纯水中25℃时的c(H+)比100℃时的c(H+)大
B. 25℃时某溶液中由水电离产生的c( H+)> =1×10-ll molL-1,则该溶液的pH可能是11或3
C. 将pH = 9的Ba(OH)2溶液与pH =4的稀盐酸混合,并保持100 ℃的恒温,混合溶液的PH=7,则此Ba(OH)2的溶液和盐酸的体积比为10:1
D. 100℃时,某 NaS04 溶液中 c(S042- ) =5 ×10 -4mol L-1,则溶液中 c(Na+): c(OH-)为104:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZulemaBorjas等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是( )
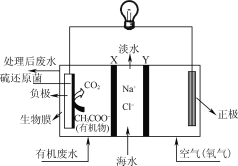
A. 该装置可以在高温下工作
B. X、Y依次为阳离子、阴离子选择性交换膜
C. 负极反应为CH3COO-+2H2O-8e-=2CO2↑+7H+
D. 该装置工作时,电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是( )
A.“青矾(绿矾)厂气熏人,衣服当之易烂,栽木不盛”。青矾厂气是![]() 和
和![]()
B.杜康用高粱酿酒的原理是通过蒸馏法将高粱中的乙醇分离出来
C.“信州铅山县有苦泉,流以为涧。挹其水熬之,则成胆矾”,其中涉及的操作有结晶
D.推广使用煤液化技术可以减少温室气体二氧化碳的排放
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com