
| A. | 离子的还原性强弱:Iˉ>Fe2+>Clˉ | |
| B. | 当a≥b时,发生的离子反应:2Fe2++Cl2=2Fe3++2Clˉ | |
| C. | 当a=b时,反应后的离子浓度之比:c(Fe2+):c(Clˉ)=1:2 | |
| D. | 当3a≤2b时,发生的离子反应:2Fe2++4Iˉ+3Cl2=2Fe3++2I2+6Clˉ |
分析 A.已知氧化性:Fe3+>I2,根据强弱规律,则还原性I->Fe2+,2Fe2++Cl2=2Fe3++2Cl-中,还原剂是Fe2+,还原产物是Cl-,则还原性Fe2+>Cl-,所以离子的还原性为:I->Fe2+>Cl-;
B.氯气与碘亚铁反应首先与还原强的碘离子反应,后与亚铁离子反应;
C.当a=b时,FeI2溶液中碘离子恰好与氯气完全反应;
D.当3a=2b时,a mol的FeI2溶液和b mol Cl2恰好完全反应.
解答 解:A.已知氧化性:Fe3+>I2,根据强弱规律,则还原性I->Fe2+,2Fe2++Cl2=2Fe3++2Cl-中,还原剂是Fe2+,还原产物是Cl-,则还原性Fe2+>Cl-,所以离子的还原性为:I->Fe2+>Cl-,故A正确;
B.氯气与碘亚铁反应首先与还原强的碘离子反应,后与亚铁离子反应,如果a=b时,FeI2溶液中碘离子恰好与氯气完全反应,则a>b时,说明只发生碘离子与氯气的反应,发生的离子反应:2I-+Cl2═I2+2Cl-,故B错误;
C、当a=b时,FeI2溶液中碘离子恰好与氯气完全反应,离子反应方程式为:2I-+Cl2═I2+2Cl-,故C正确;
D、当3a=2b时,a mol的FeI2溶液和b mol Cl2恰好完全反应,其中亚铁离子与碘离子的物质的量之比为:1:2,离子反应方程式为:2Fe2++4I-+3Cl2═2Fe3++2I2+6Cl-,故D正确;
故选B.
点评 本题以氯气和碘化亚铁的反应为载体考查了氧化还原反应,为高频考点,侧重考查学生的分析能力,明确溶液中离子反应的先后顺序是解本题的关键,采用极值讨论法来分析解答较简便,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| B. | 足量的CO2通入饱和碳酸钠溶液中:CO2+2Na++CO32-+H2O=2NaHCO3↓ | |
| C. | 酸性高锰酸钾溶液与草酸反应:2MnO4-+8H++3C2O42-=6CO2↑+2MnO2+4H2O | |
| D. | 向碳酸氢钠溶液中滴入少量澄清石灰水:Ca2++OH-+HCO3-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子中原子核内的质子数和中子数一定相等 | |
| B. | 同种元素的原子和离子核外电子数相等 | |
| C. | 化学反应前后,同种元素的原子数目一定相等 | |
| D. | 把一定量的食盐放入水中,得到溶液的质量与食盐和水的总质量一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
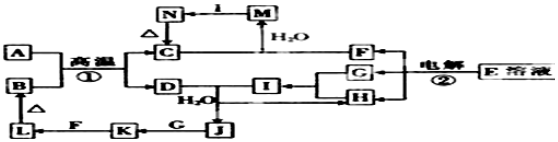
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 灼热的碳与高温水蒸气的反应 | ||
| C. | 铝与稀盐酸 | D. | H2与O2的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由“HF和NH3的水溶液都能导电”,推知二者均为电解质 | |
| B. | 由“某过程发生化学键的断裂”,推知该过程有新物质生成 | |
| C. | 由“化合物是由不同种元素组成的纯净物”,推知只含一种元素的物质一定不是化合物 | |
| D. | 由“同主族元素性质相似,CO2由分子构成”,可推知SiO2也由分子构成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01mol•L-1醋酸溶液 | |
| B. | 0.02mol•L-1醋酸与0.02mol•L-1NaOH溶液等体积混合液 | |
| C. | 过量CO2通入到0.01mol•L-1NaOH溶液后所得溶液 | |
| D. | pH=2的盐酸与pH=12的NaOH溶液等体积混合液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com