
| A. | 酶是一种蛋白质 | B. | 蛋白质是有机高分子化合物 | ||
| C. | 蛋白质的基本组成单位为氨基酸 | D. | 氨基酸是羧酸,显酸性 |
分析 A.酶属于蛋白质,酶对于许多有机化学反应和生物体内进行的复杂的反应具有很强的催化作用;
B.相对分子质量在10000以上的分子为高分子化合物;
C.蛋白质水解最终生成氨基酸;
D.氨基酸含有羧基和氨基,具有酸性和碱性.
解答 解:A.酶水解最终生成氨基酸,属于蛋白质,酶对于许多有机化学反应和生物体内进行的复杂的反应具有很强的催化作用,故A正确;
B.相对分子质量在10000以上的分子为高分子化合物,蛋白质相对分子质量在10000以上,属于高分子化合物,故B正确;
C.蛋白质水解最终生成氨基酸,所以形成蛋白质的单体是氨基酸,所以蛋白质的基本组成单位为氨基酸,故C正确;
D.氨基酸含有羧基和氨基,羧基具有酸的性质、氨基具有碱的性质,所以具有酸性和碱性,但氨基酸不属于羧酸,故D错误;
故选D.
点评 本题以氨基酸、蛋白质为载体考查有机物结构和性质,为高频考点,明确基本概念、物质结构和性质是解本题关键,易错选项是D,氨基酸具有羧基但不属于羧酸,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 只有④能证明 | B. | 都不能证明 | C. | ③④均能证明 | D. | 都能证明 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
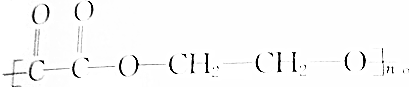 ,1mol该物质与足量NaOH溶液反应,消耗NaOH的物质的量为( )
,1mol该物质与足量NaOH溶液反应,消耗NaOH的物质的量为( )| A. | 2mol | B. | 4mol | C. | 2nmol | D. | 4nmol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=2的溶液 | B. | c(H+)=1×10-7mol/L的溶液 | ||
| C. | c(OH-)=1×10-5mol/L的溶液 | D. | pH=9的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
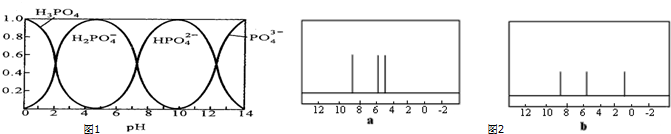
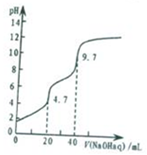 常温下,用0.1000mol•L-1 NaOH溶液滴定20mL0.1000mol•L-1 H3PO4溶液,滴定曲线如图所示,下列说法错误的是( )
常温下,用0.1000mol•L-1 NaOH溶液滴定20mL0.1000mol•L-1 H3PO4溶液,滴定曲线如图所示,下列说法错误的是( )| A. | NaH2PO4溶液呈酸性 | |
| B. | pH=9.7处,c(Na+)>c(HPO42-)>c(OH-)>c(H+) | |
| C. | pH=4.7处,c(Na+)=c(H2PO4-)+c(HPO42-)+c(PO43-) | |
| D. | 当2<pH<4.7时,H3PO4的第一步电离平衡常数均相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S$→_{点燃}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$ H2SO4 | |
| B. | Fe $→_{点燃}^{Cl_{2}}$ FeCl2$\stackrel{NaOH溶液}{→}$ Fe(OH)2 | |
| C. | AlCl3(溶液)$\stackrel{蒸发}{→}$ AlCl3$\stackrel{电解}{→}$ Al | |
| D. | NaCl(饱和溶液)$\stackrel{依次通入NH_{3}、CO_{2}}{→}$ NaHCO3$\stackrel{△}{→}$Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;分子N中含有2个手性碳原子.
;分子N中含有2个手性碳原子.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com