

| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)×(10-4mol•L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| C(CO)×(10-3mol•L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

分析 (1)①按顺序将三个热化学方程式编号为①②③,根据盖斯定律③×2-①-②可得;
②反应焓变=反应物键能总和-生成物键能总和;
(2)①依据化学反应速率是利用单位时间物质浓度的变化计算得到;
②依据图表数据结合平衡三段式列式计算平衡浓度,依据平衡常数概念分析计算得到;
③依据反应自发进行的判断依据分析△H-T△S<0,反应自发进行;
(3)A.负极的电极反应式为:CO+O2--2e-═CO2;
B.该燃料电池的正极反应为:O2+4e-=2O2-,生成的O2-由b极向a极迁移;
C.a电极是负极,b电极是正极,工作时电子由电极a通过传感器流向电极b;
D.传感器中通过的电流越大,尾气中CO的含量越高.
解答 解:(1)①按顺序将三个热化学方程式编号为①②③,根据盖斯定律③×2-自发进行①-②可得2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5 kJ•mol-1.
故答案为:-746.5 kJ•mol-1;
②N2、O2分子中化学键的键能分别是946kJ•mol-1、497kJ•mol-1,反应焓变=反应物键能总和-生成物键能总和,N2(g)+O2(g)═2NO(g)△H=+180.5kJ•mol-1
设NO分子中化学键的键能为x
△H=946kJ•mol-1++497kJ•mol-1-2x=+180.5kJ•mol-1
则NO分子中化学键的键能x=631.25kJ•mol-1
故答案为:631.25;
(2)①v (N2)=$\frac{1}{2}$v (NO)=$\frac{1}{2}$×$\frac{{10.0×{{10}^{-4}}-1.5×{{10}^{-4}}}}{3}$=1.42×10-4mol•L-1•s-1
故答案为:1.42×10-4mol•L-1•s-1;
②反应至4s达平衡,此时
c(N2)=$\frac{1}{2}$△c(NO)=$\frac{1}{2}$×(10.0×10-4 mol•L-1-1.00×10-4 mol•L-1)=4.50×10-4 mol•L-1
c(CO2)=△c(NO)=10.0×10-4 mol•L-1-1.00×10-4 mol•L-1=9.00×10-4 mol•L-1
故化学平衡常数为:K=$\frac{c({N}_{2}){c}^{2}(C{O}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$=$\frac{4.5×1{0}^{-4}mol/L×(9×1{0}^{-4}mol/L)^{2}}{(1×1{0}^{-4})^{2}×(2.7×1{0}^{-3})^{2}}$=5000L•mol-1.
故答案为:5000;
③2NO(g)+2CO(g)═N2(g)+2CO2(g)反应熵变△S<0,低温反应自发进行
故答案为:<;低温;
(3)A.负极的电极反应式为:CO+O2--2e-═CO2,故A正确;
B.该燃料电池的正极反应为:O2+4e-=2O2-,生成的O2-由b极向a极迁移,故B错误;
C.a电极是负极,b电极是正极,工作时电子由电极a通过传感器流向电极b,故C正确;
D.传感器中通过的电流越大,尾气中CO的含量越高,故D正确;
故答案为:B.
点评 本题考查较为综合,涉及热化学方程式和盖斯定律的计算应用,为高频考点,侧重于学生的分析能力和计算能力的考查,题目涉及化学反应速率,化学平衡常数的计算应用,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 英国道尔顿----提出元素概念 | |
| B. | 法国拉瓦锡----提出原子学说 | |
| C. | 俄国门捷列夫---发现元素周期律 | |
| D. | 英国波义耳----建立燃烧现象的氧化学说 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、SO42-、HCO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | Na+、K+、SO42-、Cl- | D. | NH4+、K+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
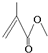 ,它的分子式为C5H8O2,存在的官能团有碳碳双键和酯基,该物质能发生的反应类型有加成反应、氧化反应、水解反应.
,它的分子式为C5H8O2,存在的官能团有碳碳双键和酯基,该物质能发生的反应类型有加成反应、氧化反应、水解反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
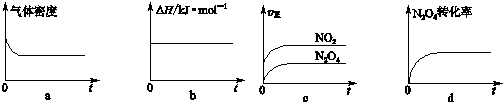
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
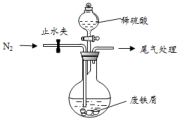 医疗上绿矾(FeSO4•7H2O)是治疗缺铁性贫血的特效药.某化学兴趣小组对绿矾进行了如下的探究:
医疗上绿矾(FeSO4•7H2O)是治疗缺铁性贫血的特效药.某化学兴趣小组对绿矾进行了如下的探究:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 编号 | 1 | 2 | 3 | 4 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 17.13 | 20.03 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
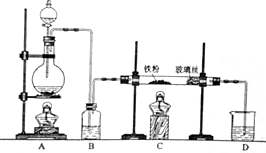 某研究性学习小组模拟工业生产过程进行试验.请回答下列问题:
某研究性学习小组模拟工业生产过程进行试验.请回答下列问题: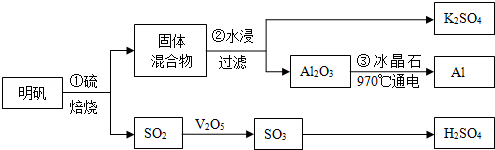
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com